题目内容
【题目】下列说法正确的是( )
A.0.1mol/LCH3COOH溶液加水稀释,溶液中c(OH﹣)增大
B.将NaOH和氨水溶液各稀释一倍,两者的OH﹣浓度均减少到原来的 ![]()
C.相同浓度的HCl和CH3COOH,两溶液中c(H+)相同
D.甲溶液的pH是5,乙溶液的pH是4,则甲溶液与乙溶液的中c(H+)之比为10:1
【答案】A
【解析】解:A、醋酸加水稀释,溶液酸性减弱,氢离子浓度减小,氢氧根离子浓度增大,故A正确;
B、将NaOH溶液和氨水溶液各稀释一倍,氢氧化钠溶液的OH﹣浓度减少到原来的二分之一,一水合氨存在电离平衡,稀释一倍,电离平衡正向进行,一水合氨溶液的OH﹣浓度大于原来的二分之一,故B错误;
C、盐酸是强酸,醋酸是弱酸存在电离平衡,如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度比醋酸溶液中氢离子浓度的二倍大,故C错误;
D、甲溶液的pH是5,溶液的c(H+)=10﹣5mol/L,乙溶液的pH是4,溶液的c(H+)=10﹣4mol/L,则甲溶液与乙溶液的c(H+)之比为10﹣5mol/L:10﹣4mol/L=1:10,故D错误;
故选A.
【考点精析】本题主要考查了弱电解质在水溶液中的电离平衡的相关知识点,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能正确解答此题.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2 , 该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
请回答下列问题:
(1)写出上述反应的化学方程式
(2)该反应的正反应是反应(填“放热”或者“吸热”),
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度/(molL﹣1) | 0.54 | 0.68 | 0.68 |
①此时系统温度400℃,比较正、逆反应速率的大小:v正v逆 (填“>”、“<”或“=”).
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中点.比较图中B、D两点所对应的正反应速率BD(填“>”、“<”或“=”).理由是 . 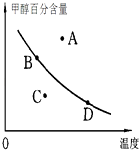
(4)一定条件下要提高反应物的转化率,可以采用的措施是
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物.