题目内容
下列各组物质中,Y是X物质中含有的少量杂质,Z是除杂试剂,其中所加试剂最合理的一组是
| | X | Y | Z |
| A | NaHCO3溶液 | Na2CO3 | BaCl2溶液 |
| B | FeCl3溶液 | CuCl2 | Fe |
| C | Fe2O3 | Al2O3 | NaOH溶液 |
| D | Na2SO4溶液 | Na2CO3 | 盐酸 |
C
试题分析:A、加BaCl2溶液除去 Na2CO3 ,引入新杂质Cl-,不合理;B、加入Fe可以与FeCl3 反应,不合理;C、加入NaOH溶液只与Al2O3 反应,合理;D、加入盐酸,引入新杂质,不合理。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目




 Mg(ClO3)2+2NaCl↓,
Mg(ClO3)2+2NaCl↓, 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O 2KMnO4+2KOH+H2↑。与原方法相比,电解法的优势为 。
2KMnO4+2KOH+H2↑。与原方法相比,电解法的优势为 。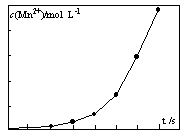
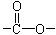 键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为
键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为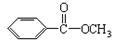 )是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成。实验室现以食品防腐剂[主要成分为苯甲酸钠(
)是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成。实验室现以食品防腐剂[主要成分为苯甲酸钠(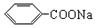 )]、甲醇为原料制备苯甲酸甲酯。已知:
)]、甲醇为原料制备苯甲酸甲酯。已知: