题目内容
【题目】右图为Mg——NaClO燃料电池结构示意图。下列说法正确的是
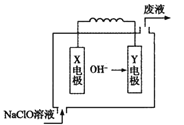
A.镁作Y电极
B.电池工作时Na+向负极移动
C.废液的pH大于NaClO溶液的pH
D.X电极上发生的反应为:ClO-+2H2O-4e-=ClO3-+4H+
【答案】A
【解析】
试题分析:A、镁是活泼的金属,次氯酸钠具有强氧化性,镁失去电子,作负极,原电池中阳离子向正极移动,阴离子向负极移动,则Y电极是负极,即Y是镁,A正确;B、原电池中阳离子向正极移动,则电池工作时Na+向正极移动,B错误;C、负极镁失去电子与溶液中的氢氧根结合生成氢氧化镁沉淀,所以反应后溶液的碱性降低,C错误;D、X电极是正极,得到电子,则X电极上发生的反应为:ClO-+H2O+2e-=Cl-+2OH-,D错误,答案选A。

练习册系列答案
相关题目
【题目】仔细分析下列表格中烃的排列规律,判断排列在第16位烃的分子式是( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | …… |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | …… |
A.C6H12 B.C6H14 C.C7H12 D.C7H14