题目内容
(9分) A、B、C、D是中学化学中常见的四种短周期元素。已知①A具有多种同素异形体,A元素原子最外层电子数是次外层电子数的2倍。②B元素最高正价为 + 5。③C元素有多种化合价,且常温下C元素的单质与某种一元碱溶液反应,可得到两种含C元素的化合物。④B、C两种元素质子数之和是A元素质子数的4倍。⑤D是地壳中含量第二的元素,它的单质是一种良好的半导体材料。
(1) 写出A元素的名称_________和C离子的结构示意图____________。
(2) 工业上利用A的单质来制备单质D,请写出相应的方程式:
________________________________________________________________________。
(3) 由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种见的漂白性物质和一种能使石蕊试纸变蓝的气体。则X的分子式 。X分子中B、C原子间的化学键的类型为___________(填“极性键”或“非极性键”)。X与水反应的化学方程式________________________。
(1) 写出A元素的名称_________和C离子的结构示意图____________。
(2) 工业上利用A的单质来制备单质D,请写出相应的方程式:
________________________________________________________________________。
(3) 由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种见的漂白性物质和一种能使石蕊试纸变蓝的气体。则X的分子式 。X分子中B、C原子间的化学键的类型为___________(填“极性键”或“非极性键”)。X与水反应的化学方程式________________________。
(9分) (1) 碳(1分) 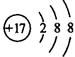 (1分)
(1分)
(2) SiO2 + 2C Si + 2CO↑(2分)
Si + 2CO↑(2分)
(3) NCl3(2分) 极性键(1分) NCl3 + 3H2O = NH3↑+ 3HClO(2分)
 (1分)
(1分)(2) SiO2 + 2C
 Si + 2CO↑(2分)
Si + 2CO↑(2分)(3) NCl3(2分) 极性键(1分) NCl3 + 3H2O = NH3↑+ 3HClO(2分)
略

练习册系列答案
相关题目
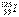 治疗肿瘤,该核素原子核内的中子数与电子数之差是
治疗肿瘤,该核素原子核内的中子数与电子数之差是