��Ŀ����
11�� ��֪A��B��C��D��Ϊǰ������Ԫ����ԭ��������������Ԫ��A�Ļ�̬ԭ��2p�����3��δ�ɶԵ��ӣ�Ԫ��B��ԭ�����������������ڲ��������3����Ԫ��C��һ�ֳ�������Ϊ����ɫ��ĩ��D���ڲ���ȫ���������ӣ�������������Ϊl��
��֪A��B��C��D��Ϊǰ������Ԫ����ԭ��������������Ԫ��A�Ļ�̬ԭ��2p�����3��δ�ɶԵ��ӣ�Ԫ��B��ԭ�����������������ڲ��������3����Ԫ��C��һ�ֳ�������Ϊ����ɫ��ĩ��D���ڲ���ȫ���������ӣ�������������Ϊl����1���ڵ�2�����У���һ�����ܴ���A��Ԫ����2�֣�
��2��CB2���ӵĿռ乹��ΪV�Σ�H2B���Ҵ��е��ܽ�ȴ���H2C����ԭ����ˮ�������Ҵ�����֮���γ������
��3��AB3-�У�Aԭ�ӹ�����ӻ�������sp2����AB3-��Ϊ�ȵ��������Ļ�ѧʽΪSO3��BF3��CO32-��SiO32-�ȣ�д��һ�ּ��ɣ���
��4��D��OH��2������ˮ�������ڰ�ˮ��д�������ڰ�ˮ�����ӷ���ʽ��Cu��OH��2+4NH3��H2O=[Cu��NH3��4]2++2OH-+4H2O��
��5��D2B�ľ�����ͼ��ʾ����֪������ܶ�Ϊ��g/cm3�������ӵ�����ΪNA�����߳�Ϊ$\root{3}{\frac{288}{��{N}_{A}}}$cm���ú�r��NA��ʽ�ӱ�ʾ����
���� A��B��C��D��Ϊǰ������Ԫ����ԭ��������������Ԫ��A�Ļ�̬ԭ��2p�����3��δ�ɶԵ��ӣ���������Ų�Ϊ1s22s22p3����AΪNԪ�أ�Ԫ��B��ԭ�����������������ڲ��������3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����BΪOԪ�أ�Ԫ��C��һ�ֳ�������Ϊ����ɫ��ĩ����CΪSԪ�أ�D���ڲ���ȫ���������ӣ�������������Ϊl��ԭ����������S��ֻ�ܴ��ڵ������ڣ����������=2+8+18+1=29����DΪCuԪ�أ��ݴ˽��
��� �⣺A��B��C��D��Ϊǰ������Ԫ����ԭ��������������Ԫ��A�Ļ�̬ԭ��2p�����3��δ�ɶԵ��ӣ���������Ų�Ϊ1s22s22p3����AΪNԪ�أ�Ԫ��B��ԭ�����������������ڲ��������3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����BΪOԪ�أ�Ԫ��C��һ�ֳ�������Ϊ����ɫ��ĩ����CΪSԪ�أ�D���ڲ���ȫ���������ӣ�������������Ϊl��ԭ����������S��ֻ�ܴ��ڵ������ڣ����������=2+8+18+1=29����DΪCuԪ�أ�
��1��ͬ������ԭ����������Ԫ�ص�һ�����ܳ��������ƣ�����Ԫ��ԭ��2p�������3�����ӣ�Ϊ�����ȶ�״̬�������ϵͣ���һ�����ܸ���OԪ�أ����Եڶ�������F��Ne�ĵ�һ�����ܶ�����NԪ�أ�
�ʴ�Ϊ��2��
��2��CB2����ΪSO2����������ԭ�ӵļ۲���Ӷ�Ϊ$\frac{6}{2}$=3����һ�Թµ��Ӷԣ����Է��ӵĿռ乹��ΪV�Σ�ˮ�������Ҵ�����֮���γ��������H2O���Ҵ��е��ܽ�ȴ���H2S��
�ʴ�Ϊ��V�Σ�ˮ�������Ҵ�����֮���γ������
��3��NO3-��Nԭ�Ӽ۲���Ӷ���=3+$\frac{5+1-2��3}{2}$=3��Nԭ�ӹ�����ӻ�������sp2����NO3-��Ϊ�ȵ��������Ļ�ѧʽΪSO3��BF3��CO32-��SiO32-�ȣ�
�ʴ�Ϊ��sp2��SO3��BF3��CO32-��SiO32-�ȣ�
��4��Cu��OH��2������ˮ�������ڰ�ˮ�������ڰ�ˮ�����ӷ���ʽΪ��Cu��OH��2+4NH3��H2O=[Cu��NH3��4]2++2OH-+4H2O��
�ʴ�Ϊ��Cu��OH��2+4NH3��H2O=[Cu��NH3��4]2++2OH-+4H2O��
��5��Cu2O�ľ����к�ɫ����Ŀ=4����ɫ����Ŀ=2+8��$\frac{1}{8}$=2���ʺ�ɫ��ΪCu����ɫ��ΪO����������=2��$\frac{64��2+16}{{N}_{A}}$g��������ܶ�Ϊ�� g•cm-3�������=$\frac{\frac{64��2+16}{{N}_{A}}��2}{��}$cm3=$\frac{288}{��{N}_{A}}$cm3�����߳�=$\root{3}{\frac{288}{��{N}_{A}}}$cm��
�ʴ�Ϊ��$\root{3}{\frac{288}{��{N}_{A}}}$��
���� �����Ƕ����ʽṹ�Ŀ��飬�漰�����ܡ����ӽṹ���ӻ�������ȵ����塢������������ȣ��ƶ�Ԫ���ǽ���ؼ�����Ҫѧ���߱���ʵ�Ļ������Ѷ��еȣ�

| A�� | ��n=4����X�ǵ�������Ԫ�� | |
| B�� | ��n=3����Z���ܵ���25 | |
| C�� | ��X�ǵ�������Ԫ�أ�����С�ns2np6nd5���Ų���ԭ��һ��ֻ��2�� | |
| D�� | ��n=4����X�Ļ�̬ԭ��һ����10��s���� |
| A�� | ����� ���Ӽ��������� �Ǽ��Լ� | |
| B�� | ����� ����� ���Լ� | |
| C�� | ����� ���Լ��� ���Ӽ������� | |
| D�� | ���Ӽ��������� ����� �Ǽ��Լ� |
������I2��g��+H2��g��?2HI��g����H=-9.48kJ/mol
������I2��s��+H2��g��?2HI��g����H=+26.48kJ/mol
�����ж���ȷ���ǣ�������
| A�� | 254 g I2��g����ͨ��2 g H2��g������Ӧ����9.48 kJ | |
| B�� | 1 mol��̬����1 mol��̬���������������17.00 kJ | |
| C�� | ��Ӧ�������ķ�Ӧ���������ȷ�Ӧ�������ķ�Ӧ���������� | |
| D�� | ��Ӧ�������IJ���ȷ�Ӧ�������IJ����ȶ� |
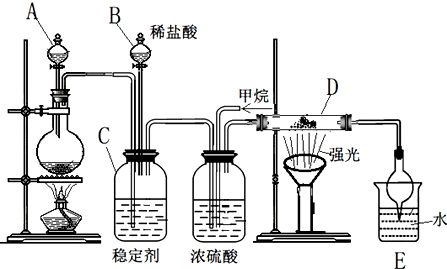
 C��SiԪ���ڻ�ѧ��ռ�м�����Ҫ�ĵ�λ��
C��SiԪ���ڻ�ѧ��ռ�м�����Ҫ�ĵ�λ��