题目内容
T℃时,某NaOH溶液中c(H+)=10-a mol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如表中所示:
假设溶液混合前后的体积变化忽略不计,则c为 ( )
A.3 B.4 C.5 D.6
| 序号 | NaOH溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 20.00 | 0.00 | 8 |
| ② | 20.00 | 20.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则c为 ( )
A.3 B.4 C.5 D.6
B
由题意可知在该温度下水的离子积常数为1×10-12,通过①可知此NaOH溶液中c(OH-)=1×10-4 mol·L-1。由②可知加入20.00 mL盐酸后溶液的pH=6,此时恰好完全中和,则c(H+)=0.0200 L×1×10-4 mol·L-1/0.0200 L=1×10-4 mol·L-1,则c=4。

练习册系列答案
相关题目
 2CO(g) ΔH="-221" kJ·mol-1
2CO(g) ΔH="-221" kJ·mol-1
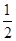 O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1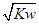 mol·L-1
mol·L-1