��Ŀ����
����Ŀ����NAΪ����٤������ֵ�������й���������ȷ����: ( )
A. 5.8g��ʯ�ࣨ2CaSO4��H2O�����еĽᾧˮ������Ϊ0.02NA
B. ��K37ClO3+6H35Cl��Ũ��=KCl+3Cl2��+3H2O��Ӧ�У�����212���������ɣ���Ӧ�е���ת�Ƶ���ĿΪ5NA
C. 60�˵�����������ǻ������ȼ������2NA��O2
D. 1mol CnH2n-2��n��2���������Ĺ��õ��Ӷ���Ϊ��3n+1��NA
���𰸡�D
��������A .5.8g��ʯ�ࣨ2CaSO4��H2O�������ʵ���Ϊ0.02mol�����еĽᾧˮ������Ϊ0.02NA����A��ȷ��B .��K37ClO3+6H35Cl��Ũ��=KCl+3Cl2��+3H2O��Ӧ��Cl2��ƽ����Է�������Ϊ![]() =
=![]() ���ҷ�Ӧ��ÿ����3molCl2ת�Ƶ�����Ϊ5mol������212��������3mol�������ɣ���Ӧ�е���ת�Ƶ���ĿΪ5NA����B��ȷ��C .����������ǵ����ʽΪCH2O��60�˵�CH2O���ȼ������2NA��O2����C��ȷ��D .CnH2n+2��n��2���к���2n+2��̼�����n-1��̼̼�������õ��Ӷ���Ϊ3n+1�� CnH2n-2��n��2�������CnH2n+2��n��2����4��̼�����̼��̼֮��2�����Ӷԣ����õ��Ӷ�����Ϊ3n-1����1mol CnH2n-2��n��2���������Ĺ��õ��Ӷ���Ϊ��3n-1��NA����D����ΪD��
���ҷ�Ӧ��ÿ����3molCl2ת�Ƶ�����Ϊ5mol������212��������3mol�������ɣ���Ӧ�е���ת�Ƶ���ĿΪ5NA����B��ȷ��C .����������ǵ����ʽΪCH2O��60�˵�CH2O���ȼ������2NA��O2����C��ȷ��D .CnH2n+2��n��2���к���2n+2��̼�����n-1��̼̼�������õ��Ӷ���Ϊ3n+1�� CnH2n-2��n��2�������CnH2n+2��n��2����4��̼�����̼��̼֮��2�����Ӷԣ����õ��Ӷ�����Ϊ3n-1����1mol CnH2n-2��n��2���������Ĺ��õ��Ӷ���Ϊ��3n-1��NA����D����ΪD��

 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�����Ŀ������������Ӱ�����ǵ�������е���������������������������������Ҫԭ��֮һ������������������������ж��ַ�����
��1���û���̿��ԭ�����Դ����������ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO��������Ӧ��C(s)+2NO(g)![]() N2(g)+CO2(g) ��H=Q kJ��mol-1����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
N2(g)+CO2(g) ��H=Q kJ��mol-1����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
ʱ��(min) Ũ�ȣ�mol��L-1�� | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
��0��10 min�ڣ�NO��ƽ����Ӧ����v(NO)=_______________________��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K=____________��
��30 min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬�����ϱ��е������жϸı������������_______(����ĸ)��
a�������¶� b��ͨ��һ������NO
c���ʵ���С��������� d��������ʵĴ���
����30 min�������¶���T2�棬�ﵽƽ��ʱ�������У�NO��N2��CO2��Ũ��֮��Ϊ5��3��3����Q__________(�>������=����<��)0��
��2��NH3����ԭ�������SCR��������ĿǰӦ����㷺���������������ѳ���������Ӧԭ����ͼ��ʾ��
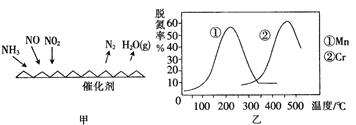
����ͼ��֪��SCR�����е�������Ϊ_______________����֪c(NO2)��c(NO)=1:1ʱ�ѵ�Ч����ѣ� ������1 mol N2ʱ��Ӧ�ų�������ΪQ kJ����ʱ��Ӧ���ѵ���Ӧ���Ȼ�ѧ����ʽΪ__________________________
��ͼ���Dz�ͬ����Mn��Cr�ڲ�ͬ�¶��¶�Ӧ���ѵ��ʣ���ͼ��֪��ҵʹ�õ���ѵĴ�������Ӧ�¶ȷֱ�Ϊ___________________________��
��3������β���е�SO2����ʯ��ˮ�����գ��������������Һ����֪������Ka1��H2SO3��=1.8��10��2 �� Ka2��H2SO3��=6.0��10��9�������£����ij��CaSO3��ˮ�γɵ���ҺpH=9������SO32���ĵڶ���ˮ�⣬��Ksp��CaSO3��=____________��
����Ŀ������ͼװ���л�����ͨ������X�����رջ�������Ʒ����Һ�ޱ仯��������ʯ��ˮ����ǣ�����������Ʒ����Һ��ɫ�����Ⱥ�V�ָ���ɫ���ݴ��ж�����X��ϴ��ƿ����ҺY�ֱ������
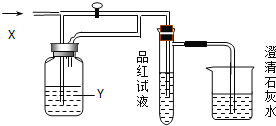
A | B | C | D | |
X | SO2 | H2S | CO2 | Cl2 |
Y | ����NaHCO3 | Ũ���� | Na2SO3 | NaHCO3 |
A. A B. B C. C D. D


