题目内容
【题目】甲醇既是重要的化工原料,又是电动公交车的清洁能源,利用水煤气在一定条件下含成甲醇,发生的反应为:![]() ?
?![]() 已知CO、
已知CO、![]() 、
、![]() 的燃烧热分别为283.0kJ/mol,285.8kJ/mol,726.5kJ/mol,则
的燃烧热分别为283.0kJ/mol,285.8kJ/mol,726.5kJ/mol,则![]() ______。
______。![]() 在一容积为2L的恒容密闭容器中加入
在一容积为2L的恒容密闭容器中加入![]() CO和
CO和![]()
![]() ,发生如下反应:CO
,发生如下反应:CO![]() ,实验测得
,实验测得![]() 和
和![]() 下,甲醇的物质的量随时间的变化如表所示,下列说法正确的是
下,甲醇的物质的量随时间的变化如表所示,下列说法正确的是
时间 | 10min | 20min | 30min | 40min | 50min | 60min |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
![]() 由上述数据可以判断:
由上述数据可以判断:![]() ______
______![]()
![]() 时,
时,![]() 的平均反应速率
的平均反应速率![]() ______。
______。![]() 该反应
该反应![]() 达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是______
达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是______![]() 选填编号
选填编号![]() 。
。
A 改用高效催化剂![]() 升高溫度
升高溫度![]() 缩小容器体积
缩小容器体积 ![]() 分离出甲醇
分离出甲醇 ![]() 增加CO的浓度
增加CO的浓度![]() 若保持
若保持![]() 不变,起始时加入CO、
不变,起始时加入CO、![]() 、
、![]() 的物质的量分别为amol、bmol、cmol,达到平衡时,仍与原平衡等效,则a、b、c应该满足的条件______。
的物质的量分别为amol、bmol、cmol,达到平衡时,仍与原平衡等效,则a、b、c应该满足的条件______。![]() 当反应在
当反应在![]() 达到20min时,控制体积不变,迅速将
达到20min时,控制体积不变,迅速将![]() ,
,![]() ,
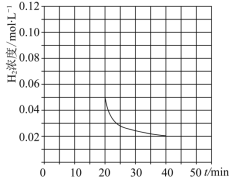
,![]() 同时投入体系中,后在恒压条件下,反应在40min时达到平衡,请在图中画出20~40min内容器中
同时投入体系中,后在恒压条件下,反应在40min时达到平衡,请在图中画出20~40min内容器中![]() 浓度的变化趋势曲线:______
浓度的变化趋势曲线:______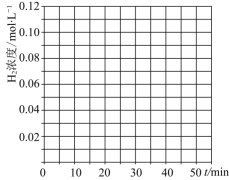
![]() 在以
在以![]() 为燃料的燃料电池中,电解质溶液为酸性,则负极的电极反应式为______;理想状态下,该燃料电池消耗2mol甲醇所能产生的最大电能为1162.4kJ,则该燃料电池的理论效率为______。
为燃料的燃料电池中,电解质溶液为酸性,则负极的电极反应式为______;理想状态下,该燃料电池消耗2mol甲醇所能产生的最大电能为1162.4kJ,则该燃料电池的理论效率为______。![]() 燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比
燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比![]()
【答案】![]()
![]()
![]() C、E
C、E ![]() ,
,![]()
![]()
![]()
【解析】
![]() 根据已知的燃烧热书写热化学方程式,推导所求反应,再根据盖斯定律计算所求反应的焓变;
根据已知的燃烧热书写热化学方程式,推导所求反应,再根据盖斯定律计算所求反应的焓变;
![]() 反应为放热反应,温度升高不利于反应正向进行;
反应为放热反应,温度升高不利于反应正向进行;
![]() 根据表中数据计算
根据表中数据计算![]() 的生成速率,再由化学反应速率之比等于化学计量数之比计算
的生成速率,再由化学反应速率之比等于化学计量数之比计算![]() 的消耗速率;
的消耗速率;
![]() 该反应
该反应![]() 达到平衡后,为同时提高反应速率和甲醇的生成量,从浓度,压强,温度角度逐项分析;
达到平衡后,为同时提高反应速率和甲醇的生成量,从浓度,压强,温度角度逐项分析;
![]() 与原平衡等效,即将反应物一边倒时,与原反应物一致;
与原平衡等效,即将反应物一边倒时,与原反应物一致;
![]() 反应为气体分子数减少的反应,随着反应进行,体系压强减小,有利于反应正向进行;
反应为气体分子数减少的反应,随着反应进行,体系压强减小,有利于反应正向进行;
![]() 原电池负极发生氧化反应,电解质溶液为酸性,
原电池负极发生氧化反应,电解质溶液为酸性,![]() 转化为
转化为![]() 和
和![]() ,据此写出负极的电极反应,根据反应的热量变化计算。
,据此写出负极的电极反应,根据反应的热量变化计算。
![]() 已知:
已知:![]() ,
,
![]() ,
,
![]() ,
,
CO![]() ,反应可由
,反应可由![]() 得到,根据盖斯定律,该反应的焓变为
得到,根据盖斯定律,该反应的焓变为![]() ,
,
故答案为:![]() ;
;
![]() 反应为放热反应,温度升高不利于反应正向进行,平衡时甲醇含量降低,所以温度
反应为放热反应,温度升高不利于反应正向进行,平衡时甲醇含量降低,所以温度![]() ,
,
故答案为:![]() ;
;
![]() 时,
时,![]() 内,
内,![]() 的生成速率为
的生成速率为![]() ,由化学反应速率之比等于化学计量数之比,则
,由化学反应速率之比等于化学计量数之比,则![]() 的消耗速率为
的消耗速率为![]() ,
,
故答案为:![]() ;
;
![]() 改用高效催化剂,催化剂只能改变化学反应速率,但不改变化学平衡,故A不选;
改用高效催化剂,催化剂只能改变化学反应速率,但不改变化学平衡,故A不选;
B.升高温度有利于加快化学反应速率,但不利于反应正向进行,不利于提高![]() 产量,故B不选;
产量,故B不选;
C.缩小容器体积相当于加压,有利于加快化学反应速率,有利于反应正向进行,即有利于提高![]() 产量,故C选;
产量,故C选;
D.分离出甲醇减小逆反应速率,瞬时不改变正反应速率,有利于反应正向进行,故D不选;
E.增加CO的浓度增大正反应速率,瞬时速率不变,但随之不断增大达到新平衡,有利于反应正向进行,即有利于提高![]() 产量,故E选,
产量,故E选,
故答案为:C、E;
![]() 温度下,平衡时
温度下,平衡时![]() ,则
,则![]() ,
,![]() ,保持
,保持![]() 不变,起始时加入CO、
不变,起始时加入CO、![]() 、
、![]() 的物质的量分别为amol、bmol、cmol,达到平衡时,仍与原平衡等效,将反应物一边倒,等效为起始时
的物质的量分别为amol、bmol、cmol,达到平衡时,仍与原平衡等效,将反应物一边倒,等效为起始时![]() ,
,![]() ,则
,则![]() ,
,![]() ,
,
故答案为:![]() ,
,![]() ;
;
![]() 反应为气体分子数减少的反应,随着反应进行,体系压强减小,有利于反应正向进行,所以恒压条件下,反应在40min时达到平衡,变化趋势图为:
反应为气体分子数减少的反应,随着反应进行,体系压强减小,有利于反应正向进行,所以恒压条件下,反应在40min时达到平衡,变化趋势图为: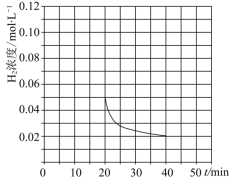 ,
,
故答案为: ;
;
![]() 原电池负极发生氧化反应,电解质溶液为酸性,
原电池负极发生氧化反应,电解质溶液为酸性,![]() 转化为
转化为![]() 和
和![]() ,则负极的电极反应为:
,则负极的电极反应为:![]() ,理想状态下,该燃料电池消耗2mol甲醇所能产生的最大电能为1162.4kJ,2mol甲醇完全燃烧释放的热量为
,理想状态下,该燃料电池消耗2mol甲醇所能产生的最大电能为1162.4kJ,2mol甲醇完全燃烧释放的热量为![]() ,所以该燃料电池的理论效率为
,所以该燃料电池的理论效率为![]() ,
,
故答案为:![]() ;
;![]() 。
。

【题目】碳和氮的化合物在生产生活中广泛存在。回答下列问题:![]() 三氯化氮
三氯化氮![]() 是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是______。氯碱工业生产时,由于食盐水中通常含有少量
是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是______。氯碱工业生产时,由于食盐水中通常含有少量![]() ,而在阴极区与生成的氯气反应产生少量
,而在阴极区与生成的氯气反应产生少量![]() ,该反应的化学方程式为______。
,该反应的化学方程式为______。![]() 一定条件下,不同物质的量的
一定条件下,不同物质的量的![]() 与不同体积的
与不同体积的![]() 溶液充分反应放出的热量如下表所示:
溶液充分反应放出的热量如下表所示:
反应序号 | n | V | 放出的热量 |
1 |
|
| A |
2 |
|
| b |
该条件![]() 与NaOH 溶液反应生成
与NaOH 溶液反应生成![]() 的热化学反应方程式为______。
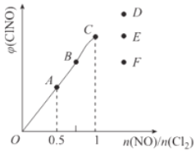
的热化学反应方程式为______。![]() 利用CO可以将NO转化为无害的
利用CO可以将NO转化为无害的 ,其反应为:
,其反应为:![]() ,向容积均为1L的甲,乙两个恒温
,向容积均为1L的甲,乙两个恒温![]() 温度分别为
温度分别为![]() 、
、![]() 容器中分别加入
容器中分别加入![]() 和
和![]() ,测得各容器中
,测得各容器中![]() 随反应时间t的变化情况如下表所示:
随反应时间t的变化情况如下表所示:
| 0 | 40 | 80 | 120 | 160 |
|
|
|
|
|
|
|
|
|
|
|
|
![]() 甲容器中,
甲容器中,![]() 内用NO的浓度变化表示的反应速率
内用NO的浓度变化表示的反应速率![]() ______。
______。![]() 该反应的
该反应的![]() ______
______![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() 。
。![]() 甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡______
甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡______![]() 填“正向”、“逆向”或“不”
填“正向”、“逆向”或“不”![]() 移动。
移动。![]() 常温下,在
常温下,在![]() 溶液中,反应
溶液中,反应![]() 的平衡常数
的平衡常数![]() ______。
______。![]() 已知常温下,
已知常温下,![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]()
![]() 在酸性电解质溶液中,以惰性材料作电极,将
在酸性电解质溶液中,以惰性材料作电极,将![]() 转化为丙烯的原理如图所示
转化为丙烯的原理如图所示

![]() 太阳能电池的负极是______
太阳能电池的负极是______![]() 填“a”或“b”
填“a”或“b”![]()
![]() 生成丙烯的电极反应式是______。
生成丙烯的电极反应式是______。
【题目】用试纸检验气体性质是一种重要的实验方法.如表所示的实验中![]() 可加热
可加热![]() ,下列试纸的选用、现象、对应结论都正确的一项是
,下列试纸的选用、现象、对应结论都正确的一项是![]()
序号 | 试剂B | 湿润的试纸A | 结论 |
A | 碘水 | 淀粉试纸变蓝 | 碘具有氧化性 |
B | 浓氨水、生石灰 | 蓝色石蕊试纸变红 | 氨气为碱性气体 |
C |
| 品红试纸褪色 |
|
D | Cu、浓硝酸 | 淀粉KI试纸变蓝 |
|
A.AB.BC.CD.D