题目内容
【题目】氢气是重要的化学试剂,化工原料和有广阔发展前景的新能源。
请回答下列问题:
I.实验室用锌和稀硫酸制备氢气时,可向稀硫酸中滴加少量硫酸铜溶液以加快反应速率,原因为____________。
II.以甲醇为原料制备氢气的一种原理如下:
i . CH3OH(g) ![]() CO(g)+2H2(g) △H=+90kJ·mol-1
CO(g)+2H2(g) △H=+90kJ·mol-1
ii. CO(g)+H2O(g)![]() CO2(g)+ H2(g) △H=-41kJ·mol-1
CO2(g)+ H2(g) △H=-41kJ·mol-1
(1)已知:断裂1 mol分子中的化学健需要吸收的能量如下表所示。

表中x =___________。
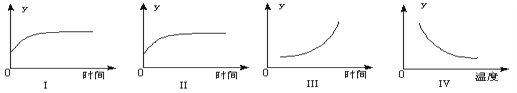
(2)向vL恒容密闭容器中充入lmo1 CH3OH(g),发生反应i,图l中能正确表示CH3OH(g)的平衡转化率(a)随温度(T)变化关系的曲线为________(填“A ”或“B”),理由为______,T1℃ 时,体系的平衡压强与起始压强之比为___________________。

(3)起始向10L恒容密闭容器中充入1 mol CH3OH(g)和1molH2O(g),发生反应i和反应ii,体系中CO的平衡体积分数与温度(T)和压强(p)的关系如图2所示。
①随着温度升高, ![]() 的值_______(填“增大”“ 减小” 或“不变”),理由为_____。
的值_______(填“增大”“ 减小” 或“不变”),理由为_____。
②P1、P2、p3由大到小的顺序为_______。
③测得C点时,体系中CO2的物质的量为0 . 2 mol,则T2℃时,反应ii的平衡常数K=_______。
【答案】 锌置换出硫酸铜中的铜,形成许多微小原电池,加快反应速率 1606 B 反应i为吸热反应,升高温度,平衡正向移动,CH3OH(g)的平衡转化率增大 9:5 减小 升高温度,反应i中CO的物质的量增大,反应ii中CO的物质的量增大、CO2的物质的量减小。最终![]() 的值减小 p3>p2>p1 0.875
的值减小 p3>p2>p1 0.875
【解析】I.实验室用锌和稀硫酸制备氢气时,可向稀硫酸中滴加少量硫酸铜溶液以加快反应速率,个原因为锌置换出硫酸铜中的铜,形成许多微小原电池,加快反应速率。
II.(1)由i . CH3OH(g) ![]() CO(g)+2H2(g) △H=+90kJ·mol-1
CO(g)+2H2(g) △H=+90kJ·mol-1
ii. CO(g)+H2O(g)![]() CO2(g)+ H2(g) △H=-41kJ·mol-1两个热化学方程式相加可得:CH3OH(g) +H2O(g)
CO2(g)+ H2(g) △H=-41kJ·mol-1两个热化学方程式相加可得:CH3OH(g) +H2O(g)![]() CO2(g) +3H2(g) △H=+49kJ·mol-1,因为△H=反应物的键能总和-生成物的键能总和=2038+925-x-436
CO2(g) +3H2(g) △H=+49kJ·mol-1,因为△H=反应物的键能总和-生成物的键能总和=2038+925-x-436![]() =49,解之得x=1066.所以表中x =1606。
=49,解之得x=1066.所以表中x =1606。
(2). 向vL恒容密闭容器中充入lmo1 CH3OH(g),发生反应i,图l中能正确表示CH3OH(g)的平衡转化率(a)随温度(T)变化关系的曲线为B,理由为反应i为吸热反应,升高温度,平衡正向移动,CH3OH(g)的平衡转化率增大,T1℃ 时,
CH3OH(g) ![]() CO(g)+2H2(g)
CO(g)+2H2(g)
起始量(mol) 1 0 0
变化量(mol) y y 2y
平衡量(mol) 1-y y 2y
由图像知CH3OH的转化率=40% = ![]()
![]() ,解之得y=
,解之得y=![]() 。在同温同压下体系的平衡压强与起始压强之比等于其物质的量之比=
。在同温同压下体系的平衡压强与起始压强之比等于其物质的量之比=![]() 9:5。
9:5。
(3).起始向10L恒容密闭容器中充入1 mol CH3OH(g)和1molH2O(g),发生反应i和反应ii,因为反应i为吸热反应,而反应ii为放热反应,所以①随着温度升高, ![]() 的值减小,理由为升高温度,反应i中平衡向右移动使CO的物质的量增大,反应ii中平衡向左移动使CO的物质的量增大、CO2的物质的量减小,最终
的值减小,理由为升高温度,反应i中平衡向右移动使CO的物质的量增大,反应ii中平衡向左移动使CO的物质的量增大、CO2的物质的量减小,最终![]() 的值减小。
的值减小。
②反应i正反应方向为气体分子增多的方向,反应ii气体分子数不变,所以压强只对反应i的化学平衡产生影响,压强增大,平衡向逆反应方向移动,CO的物质的量分数变小,所以P1、P2、p3由大到小的顺序为p3>p2>p1。
③测得C点时,体系中CO2的物质的量为0.2 mol,则T2℃时,设混合气体中n(CO)=x,则由C原子守恒,n(CH3OH)=1mol-0.2mol-x,由反应ii:
CO(g)+H2O(g)![]() CO2(g)+ H2(g)
CO2(g)+ H2(g)
起始量(mol) 1 0
变化量(mol) 0.2 0.2
平衡量(mol) 0.8 0.2
所以平衡体系中n(H2O)=0.8mol。再由H原子守恒得:
n(H2)= ![]() = 0.6mol+x
= 0.6mol+x
因为平衡体系中CO的物质的量分数为12.5%
所以![]() =12.5% ,解之得x=0.4mol
=12.5% ,解之得x=0.4mol
所以平衡体系中n(CO)=0.4mol,n(H2O)=0.8mol,n(CO2)=0.2mol,n(H2)=1.4mol,由于各组分的化学计量数都是1,所以可以直接用物质的量代替物质的量浓度计算平衡常数,反应ii的平衡常数K= ![]() =
=![]() =0.875。
=0.875。

【题目】七水硫酸镁(MgSO4·7H2O)为白色细小四角柱状结晶,无臭,味苦,在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、CaO、B2O3、Al2O3、MnO等)。
表1部分阳离子以氢氧化物形式完全沉淀时溶液的pH
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)3 | Mn(OH)2 | Mg(OH)2 |
pH值 | 4.7 | 3.2 | 9.7 | 10.4 | 11.2 |
表2两种盐的溶解度(单位为g/100g水)
温度/℃ | 10 | 30 | 40 | 50 | 60 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | — |
硼镁泥制取七水硫酸镁的工艺流程如下

根据以上流程图并参考表格数据,试回答下列问题:
(1)在酸溶过程中,想加快酸溶速度,提出两种可行的措施_______________。
(2)沉淀A中除二氧化硅外,还含有硼酸(H3BO3),硼酸微溶于水,为一元弱酸,其酸性不来源于羟基的电离,写出硼酸水溶液电离方程式____________________
(3)经对沉淀B进行分析,发现其中含有二氧化锰,用离子方程式解释产生二氧化锰原因:__________________。
(4)加入硼镁泥调节pH=5~6目的是________________。
(5)得到的沉淀C的组成是_________________(填化学式),过滤Ⅲ需趁热过滤,原因是___________。
(6)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是____________。