题目内容
下列物质含有离子键的是
| A.Cl2 | B.NaCl | C.CO2 | D.H2O |
B
解析试题分析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,则A、氯气分子氯原子与氯原子形成非极性键,A不正确;B、氯化钠中钠离子与氯离子形成离子键,B正确;C、二氧化碳中碳原子与氧原子形成共价键,C不正确;D、水分子中氢原子与氧原子形成共价键,D不正确,答案选B。
考点:考查化学键判断

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述不正确的是
A.NH4H的电子式为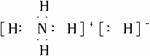 | B.NH4Cl的电子式为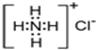 |
| C.NH4H含有极性共价键和离子键 | D.NH4H固体投入少量热水中,有两种气体生成 |
关于晶体的下列说法正确的是( )
| A.化学键都具有饱和性和方向性 |
| B.晶体中只要有阴离子,就一定有阳离子 |
| C.氢键具有方向性和饱和性,也属于一种化学键 |
| D.金属键由于无法描述其键长、键角,故不属于化学键 |
下列各组物质中,每种物质都是既有离子键又有共价键的一组是( )
| A.NaOH H2SO4 (NH4)2SO4 | B.MgO Na2SO4 HNO3 |
| C.Na2O2 KOH Na3PO4 | D.HCl Na2O MgCl2 |
下列物质中含有共价键的离子化合物是
| A.Ba(OH)2 | B.CaCl2 | C.H2O | D.H2 |
下列说法错误的是
| A.对羟基苯甲酸的沸点比邻羟基苯甲酸高,冰中既存在范德华力,又存在氢键 |
| B.简单立方是非密置层三维堆积形成的,面心立方是由密置层三维堆积形成的 |
| C.所有共价键都有方向性,形成氢键的三个相关原子可以不在直线上 |
| D.金属晶体的导电、导热性都与自由电子有关,离子晶体在一定条件下可以导电 |
下列说法正确的是( )
| A.1个甘氨酸分子中存在9对共用电子 |
| B.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
C.H2(g)+Br2(g)=2HBr(g)△H=-72 kJ·mol-1其它相关数据如下表: 则表中a为230 |
| D.已知S(g)+O2(g)=SO2(s);△H1,S(g)+O2(g)=SO2(g);△H2,则△H2<△H1 |
下列过程中没有破坏化学键的是( )
| A.氯化氢溶于水 | B.氯化铵分解 | C.食盐熔化 | D.干冰升华 |
有关物质结构的叙述中,正确的是
| A.只含有共价键的物质不一定是共价化合物 |
| B.由电子定向移动而导电的物质一定是金属晶体 |
| C.有键能很大的共价键存在的物质熔沸点一定很高 |
| D.原子晶体中只存在非极性共价键 |