题目内容
【题目】一定温度下,在一个10 L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=c(CO)c(H2)/c(H2O),请回答下列问题:
(1)该反应的化学方程式为______________________________;若温度升高, K增大,则该反应是___________ (填“吸热”或“放热”)反应。
(2)能判断该反应一定达到平衡状态的是___________(填字母序号)。
A.v正(H2O)=v逆(H2)
B.容器中气体的平均相对分子质量不随时间改变
C.消耗nmol H2的同时消耗nmol CO
D.容器中物质的总物质的量不随时间改变
(3)该反应的v(正)随时间变化的关系如图,在t2min时改变了某种条件,改变的条件可能是______、________。(写2条)

【答案】C+H2O![]() CO+H2 吸热 A B 增大反应物浓度 升高温度
CO+H2 吸热 A B 增大反应物浓度 升高温度
【解析】
(1)依据平衡常数表达式书写方法和元素守恒写出化学方程式,用生成物平衡浓度的幂次方乘积除以反应物平衡浓度幂次方乘积,平衡移动原理分析可知,温度升高,平衡常数中等,说明平衡正向进行为吸热反应;
(2)化学平衡的根本原因是正、逆反应速率相等,反应混合物中各组分的百分含量保持不变,然后根据具体的化学方程式,逐一判断;
(3)根据图象可知,t2时正反应速率立即增大,达到平衡时正反应速率大于原平衡状态时的反应速率
(1)①根据平衡常数的定义,生成物浓度的幂之积与反应物浓度的幂之积之比为平衡常数,反应的方程式为C(s)+H2O(g)CO(g)+H2(g),故答案为:C(s)+H2O(g)CO(g)+H2(g);
(2)A、v正(H2O)=v逆(H2)时,氢气正逆反应速率相同,反应达到平衡,故A正确;
B、反应前后气体的物质的量不相同,气体质量变化,容器中气体的平均相对分子质量不随时间变化即达到平衡,故B正确;
C、消耗nmolH2的同时消耗nmolCO,反应都代表逆反应,不能说明反应达到平衡状态,故C错误;
D、碳为固体,反应前后气体体积发生变化,容器中气体总物质的量不随时间变化,说明反应达到平衡状态,故D正确;故答案为:ABD;
(3)由图象可以知道,在t2时正反应速率立即增大,且达到平衡时正反应速率大于原平衡状态时的反应速率,说明达到平衡时反应物的浓度大于原平衡的浓度,根据影响反应速率的因素分析,可以加入生成物H2O(g),正反应速率会立刻增大,达到新的平衡时H2O(g)的浓度比原平衡的浓度大,反应速率增大;反应是吸热反应,也可以升高温度,正逆反应速率都增大,且达到平衡时正逆反应速率都大于原平衡的速率,故答案为:增大反应物浓度;升高温度.

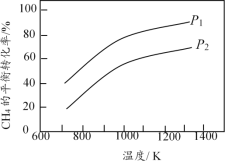
【题目】在三个容积相同的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下发生反应CH4(g)+ H2O(g) ![]() CO(g) + 3H2(g)(不发生其他反应),CH4的平衡转化率与温度、压强的关系如图所示。
CO(g) + 3H2(g)(不发生其他反应),CH4的平衡转化率与温度、压强的关系如图所示。
容器 | 起始物质的量/mol | CH4的平衡 转化率 | |||
CH4 | H2O | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.1 | 0.3 | / |
Ⅲ | 0 | 0.1 | 0.2 | 0.6 | / |
下列说法错误的是
A. 该反应的![]() H>0,图中压强P1>P2
H>0,图中压强P1>P2
B. 起始时,容器Ⅱ中v(CH4)正<v(CH4)逆
C. 达到平衡时,容器Ⅰ、Ⅱ中CO的物质的量满足:n(CO)Ⅱ< 2n(CO)Ⅰ
D. 达到平衡时,容器Ⅱ、Ⅲ中气体的总压强之比PⅡ∶PⅢ = 4∶5