题目内容
【题目】根据物质的量的有关公式计算(注:(2)(3)(4)计算结果保留小数点后两位)
(1)3.01×1023个NH4+,其质量为 g。
(2)欲配制1L 0.2 mol.L-1的盐酸溶液,需标准状况下HCl的体积为 L。
(3)现将50 mL密度为1.84 g/cm3,质量分数为98.0 %的浓硫酸,稀释至250 mL,则稀释后,溶液的物质的量浓度为 。
(4)19克MgCl2中含有离子数目 。
(5)所含原子数相等的甲烷和氨气(NH3)的质量比为 。
【答案】
(1)9(2)4.48(3)3.68 mol.L-1
(4)3.61×1023(5)64:85
【解析】
试题分析:
(1)n(NH4+)=![]() =0.5mol,m(NH4+)=0.5mol×18g/mol=9g。
=0.5mol,m(NH4+)=0.5mol×18g/mol=9g。
(2)0.2 mol.L-1的盐酸溶液1L ,那么盐酸的物质的量为 0.2×1=0.2。那么需要标准状况下HCl的体积为0.2×22.4=4.48L。
(3)物质的量浓度就是溶质的物质的量除以溶液的总体积,稀释后的溶液总体积为250 mL,而且稀释时,溶质的物质的量不变,所以硫酸物质的量就是50mL×1.84g/mL×98%÷98g/mol=0.92mol,则物质的量浓度就是0.92mol÷0.25L=3.68 mol/L。
(4)19克MgCl2的物质的量为:![]() =0.2mol,0.2mol氯化镁中含有0.2mol镁离子、0.4mol氯离子,总共含有0.6mol离子,含有离子数目0.6NA=0.6×6.02×1023=3.61×1023;
=0.2mol,0.2mol氯化镁中含有0.2mol镁离子、0.4mol氯离子,总共含有0.6mol离子,含有离子数目0.6NA=0.6×6.02×1023=3.61×1023;
(5)甲烷CH4原子数为5,氨气 NH3原子数为4,它们所含原子数相等,所以物质的量5x:4y=1:1,可知 x:y=4:5 ,质量比为(4×16):(5×17)=64:85。

【题目】甲醇是一种重要的化工原料,又是一种可再生资源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)=HCHO(g)+H2(g) △H=+84kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol
①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:________________。
②在上述制备甲醛时,常向反应器中通入适当过量的氧气,其目的是_________________。
(2)工业上可用如下方法合成甲醛,化学方程式为CO(g)+2H2(g)=CH3OH(g),已知某些化学键的键能数据如下表:
化学键 | C-C | C-H | H-H | C-O | C=O | O-H |
键能/kJ/mol | 348 | 413 | 436 | 358 | x | 463 |
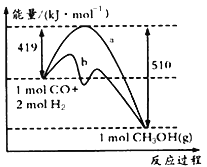
请回答下列问题:
①如图中曲线a到曲线b的措施是_______________。
②已知CO中的C与O之间为三键,其键能为xkJ/mol,则x=___________。
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池正极的电极反应式为____________________。
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/mol/L | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶液现象)阳极上收集到氧气的质量为_____________。
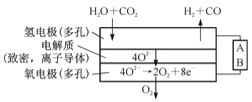
(4)电解水蒸气和CO2产生合成气(H2+CO),较高温度下(70-1000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2。由右图可知A为直流电源的 (填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:____________。