��Ŀ����
����Ŀ��ij��ѧ��ȤС���ͬѧ����ȥ��̬�Ȼ����л��е��Ȼ��ơ����������ʵ�鷽���ش�������⣺
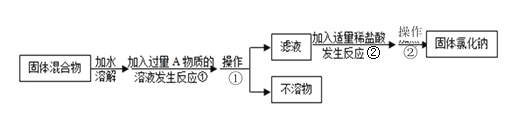
��1��������������Ҫ����������_________________________
��2����Ӧ���м����Թ�����A���ʵ�Ŀ����______________________���ж�A�ѹ�����ʵ�����������_______________________________________________����Ӧ���Ļ�ѧ��Ӧ����ʽΪ___________________________________________________��
��3��������������Ϊ__________________����Ӧ�������ӷ���ʽ______________________��
��4��ʵ��ʱ��ȡ��Ʒ����Ϊ185.0g,������������ϴ�ӡ�������ó�������Ϊ50.0g������Ʒ��NaCl�������ٷ���Ϊ_________________________����������С������һλ��
���𰸡� �ձ� ©�� ������ ��Ca2+������ȫ ���ϲ���Һ�����μ�Na2CO3��Һ������������A��������֮�������������������A���� Na2CO3 + CaCl2 = CaCO3�� + 2NaCl ���� CO32- + 2H+ = CO2��+ H2O 70.0%
���������ɷ������̿�֪���ܽ��ӹ�����Na2CO3�ɳ�ȥ�Ȼ��ƣ�������Ϊ���ˣ��õ�����Ϊ̼��ƣ���Һ�к�NaCl��������Na2CO3�����������ᣬ��ȥ̼���ƣ�������Ϊ���������õ�NaCl������
(1)���������ٵõ�����Һ�Ͳ����˵��������Ϊ���ˣ�������Ҫ�����������ձ���©�������������ʴ�Ϊ���ձ���©������������
(2)��������������AΪ̼���ơ���Ӧ���м����Թ�����A���ʵ�Ŀ���DZ�֤�����ӳ�����ȫ���ж�̼�����ѹ���ֻ��Ҫ����Һ���ú�ȡ�����ϲ���Һ���μ�������ϡ���ᣬ�����������ɣ���˵��̼�����ѹ���(��ȡ�ϲ���Һ���������μ�̼������Һ����)��̼���ƺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ���ѧ����ʽΪ��Na2CO3+CaCl2=CaCO3��+2NaCl���ʴ�Ϊ���������ӳ�����ȫ�����ú�ȡ�����ϲ���Һ���μ�������ϡ���ᣬ�����������ɣ���˵��̼�����ѹ���(�����ϲ���Һ�����μ�Na2CO3��Һ������������̼�����ѹ�������֮��̼���Ʋ���)��Na2CO3+CaCl2=CaCO3��+2NaCl��
(3)�������Ǵ��Ȼ�����Һ�еõ��Ȼ��ƹ��壬��˲�����Ϊ��������Ӧ���ǹ�����̼������ϡ����ķ�Ӧ�����ǻ��ཻ���ɷ������Ȼ��ƺ�ˮ�Ͷ�����̼�����ӷ���ʽΪ��2H++CO32-�TCO2+H2O���ʴ�Ϊ��������2H++CO32-�TCO2+H2O��
(4)��������1��ó���(������ˮ)������Ϊ50.0g����n(CaCl2)=n(CaCO3)= ![]() =0.5mol������Ʒ��NaCl������������
=0.5mol������Ʒ��NaCl������������![]() ��100%=70%���ʴ�Ϊ��70%��
��100%=70%���ʴ�Ϊ��70%��