题目内容
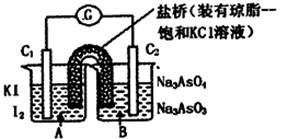
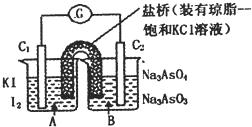 已知反应AsO43-+2I一+2H+?AsO43-+I2+H2O是可逆反应.设计如图装置(C1、C2均为石墨电极),分别进行下述操作.
已知反应AsO43-+2I一+2H+?AsO43-+I2+H2O是可逆反应.设计如图装置(C1、C2均为石墨电极),分别进行下述操作.I.向B烧杯中逐滴加入浓盐酸
II.向B烧杯中逐滴加入40%NaOH溶液结果发现电流计指针均发生偏转.
据此,下列判断正确的是( )
分析:由图可知,该装置为原电池,Ⅰ、发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极;Ⅱ、发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极;
A、操作Ⅰ中发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极;
B、操作II过程中发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极,盐桥中的钾离子向A烧杯移动;
C、I操作过程中发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,发生2I--2e-=I2,C2为正极发生还原反应;
D、AsO32-和I2在水溶液中可以发生自发的氧化还原反应,在原电池的正极上发生得电子的还原反应,负极上失电子发生氧化反应,根据氧化还原反应的生成物来确定现象以及电极方程式.
A、操作Ⅰ中发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极;
B、操作II过程中发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极,盐桥中的钾离子向A烧杯移动;
C、I操作过程中发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,发生2I--2e-=I2,C2为正极发生还原反应;
D、AsO32-和I2在水溶液中可以发生自发的氧化还原反应,在原电池的正极上发生得电子的还原反应,负极上失电子发生氧化反应,根据氧化还原反应的生成物来确定现象以及电极方程式.
解答:解:A、操作Ⅰ中发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,故A错误;
B、操作II过程中发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极,盐桥中的钾离子向A烧杯移动,故B错误;
C、I操作过程中发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,发生2I--2e-=I2,C2为正极发生还原反应,电极反应为AsO42-+2H++2e-=AsO32-+H2O,故C正确;
D、II操作过程中当向B中加入NaOH溶液时,反应AsO43-+2I-+2H+?AsO33-+I2+H2O,逆向进行,C2棒为负极失电子发生电极反应为AsO33-+H2O-2e-=AsO43-+2H+,C1为正极,电极反应为,I2+2e-=2I-,故D错误;
故选C.
B、操作II过程中发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极,盐桥中的钾离子向A烧杯移动,故B错误;
C、I操作过程中发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,发生2I--2e-=I2,C2为正极发生还原反应,电极反应为AsO42-+2H++2e-=AsO32-+H2O,故C正确;
D、II操作过程中当向B中加入NaOH溶液时,反应AsO43-+2I-+2H+?AsO33-+I2+H2O,逆向进行,C2棒为负极失电子发生电极反应为AsO33-+H2O-2e-=AsO43-+2H+,C1为正极,电极反应为,I2+2e-=2I-,故D错误;
故选C.
点评:本题考查电解池和原电池,明确电解质的不同发生的电池反应不同是解答本题的关键,并熟悉原电池和电解池的工作原理来解答即可,题目难度中等.

练习册系列答案
相关题目
已知反应AsO43-+2I-+2H+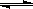 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。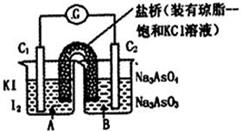
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是
| A.操作Ⅰ过程中,C1为正极 |
| B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 |
| C.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e - = AsO33-+H2O |
| D.Ⅱ操作过程中,C1棒上发生的反应为:2I- - 2e- = I2 |
 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。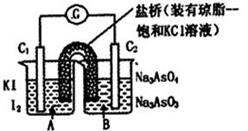
 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。