题目内容
10.有机物A、B、C、D只含有碳、氢、氧元素中的两种或三种,且它们具有相同的最简式.取A、B、C、D的混合物共3.0g在足量的O2中充分燃烧.将燃烧后的气体通过足量的浓硫酸,浓硫酸质量增加1.8g,将剩余气体通过足量澄清石灰水,得到10g沉淀.(1)上述有机物的最简式为:CH2O.
(2)有机物A在常温下呈气态,则A的结构式为:
 .
.(3)有机物B蒸气的密度是同温同压下氢气的30倍,且B能与NaHCO3溶液反应生成CO2,则B的名称为:乙酸.
(4)有机物C是B的同分异构体,C既能发生银镜反应又能发生水解反应,写出C与NaOH溶液共热时发生反应的方程式:HCOOCH3+NaOH$\stackrel{△}{→}$HCOONa+HOCH3.
(5)D的相对分子质量是A的3倍,D中有两种官能团,既能和乙酸又能和乙醇发生酯化反应,两分子D在浓硫酸作用下失去两分子水并形成一种六元化合物,D的结构简式为:CH3CH(OH)COOH.
分析 A、B、C、D具有相同的最简式,A、B、C、D的混合物共3.0g在足量的O2中充分燃烧.将燃烧后的气体通过足量的浓硫酸,浓硫酸质量增加1.8g,即得到水为0.1mol,所以有机物中氢原子的物质的量为0.2mol,将剩余气体通过足量澄清石灰水,得到10g沉淀为碳酸钙,其物质的量为0.1mol,根据碳元素守恒,生成的二氧化碳的物质的量为0.1mol,利用元素守恒可知,有机物质中氧元素的物质的量为$\frac{3.0-0.1×2+0.1×12}{16}$mol=0.1mol,所以有机物的最简式为CH2O,有机物A在常温下呈气态,则A为甲醛,B蒸气的密度是同温同压下氢气的30倍,即相对分子质量为60,且B能与NaHCO3溶液反应生成CO2,说明有羧基,所以B为乙酸,C是B的同分异构体,C既能发生银镜反应又能发生水解反应,则C为甲酸甲酯,D的相对分子质量是A的3倍,D中有两种官能团,既能和乙酸又能和乙醇发生酯化反应,两分子D在浓硫酸作用下失去两分子水并形成一种六元化合物,则D为CH3CHOHCOOH,据此答题.
解答 解:A、B、C、D具有相同的最简式,A、B、C、D的混合物共3.0g在足量的O2中充分燃烧.将燃烧后的气体通过足量的浓硫酸,浓硫酸质量增加1.8g,即得到水为0.1mol,所以有机物中氢原子的物质的量为0.2mol,将剩余气体通过足量澄清石灰水,得到10g沉淀为碳酸钙,其物质的量为0.1mol,根据碳元素守恒,生成的二氧化碳的物质的量为0.1mol,利用元素守恒可知,有机物质中氧元素的物质的量为$\frac{3.0-0.1×2+0.1×12}{16}$mol=0.1mol,所以有机物的最简式为CH2O,有机物A在常温下呈气态,则A为甲醛,B蒸气的密度是同温同压下氢气的30倍,即相对分子质量为60,且B能与NaHCO3溶液反应生成CO2,说明有羧基,所以B为乙酸,C是B的同分异构体,C既能发生银镜反应又能发生水解反应,则C为甲酸甲酯,D的相对分子质量是A的3倍,D中有两种官能团,既能和乙酸又能和乙醇发生酯化反应,两分子D在浓硫酸作用下失去两分子水并形成一种六元化合物,则D为CH3CHOHCOOH,
(1)根据上面的分析可知,上述有机物的最简式为:CH2O,故答案为:CH2O;
(2)根据上面的分析可知,A为甲醛,A的结构式为: ,故答案为:
,故答案为: ;
;
(3)根据上面的分析可知,B为乙酸,故答案为:乙酸;
(4)C为甲酸甲酯,C与NaOH溶液共热时发生反应的方程式为:HCOOCH3+NaOH$\stackrel{△}{→}$HCOONa+HOCH3,故答案为:HCOOCH3+NaOH$\stackrel{△}{→}$HCOONa+HOCH3;
(5)根据上面的分析可知,D的结构简式为:CH3CH(OH)COOH,故答案为:CH3CH(OH)COOH.
点评 本题考查有机物的确定,题目难度不大,注意从质量守恒的角度计算一氧化碳的质量,再根据原子守恒计算.

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案| X | Y | Z | |
| ① | NaOH溶液 | Al | Fe2O3 |
| ② | KOH溶液 | Br2 | Na2SO3溶液 |
| ③ | Na2CO3 | SiO2 | H2O |
| ④ | HCl | NaHCO3 | NaOH |
| A. | 只有①③④ | B. | 只有①②④ | C. | 只有①②③ | D. | ①②③④皆可 |
| A. | 氢氧化钡跟硫酸铜溶液的反应 Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓ | |
| B. | 用稀硫酸清除铁锈 Fe2O3+6H+=2Fe3++3H2O | |
| C. | 食盐水中滴加硝酸银溶液 Cl-+Ag+=AgCl↓ | |
| D. | 氢氧化铁与盐酸反应 OH-+H+=H2O |
| A. | 甲中沉淀一定比乙中的多 | B. | 甲中和乙中的沉淀一定一样多 | ||
| C. | 甲中沉淀一定比乙中的少 | D. | 甲中沉淀可能比乙中的多 |
| A. | 1mol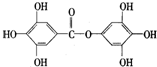 最多能与8molNaOH发生反应 最多能与8molNaOH发生反应 | |
| B. | 甲苯既能跟溴水反应又能跟酸性高锰酸钾溶液反应 | |
| C. | 向苯酚钠溶液中通入少量的CO2气体,发生反应的离子方程式为: 2 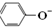 +H2O+CO2→2 +H2O+CO2→2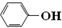 +CO${\;}_{3}^{2-}$ +CO${\;}_{3}^{2-}$ | |
| D. | 1mol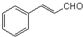 最多能和4molH2发生反应 最多能和4molH2发生反应 |
 常温下,向10mL 0.1mol•L-1的CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,所得滴定曲线如图所示.下列说法一定正确的是( )
常温下,向10mL 0.1mol•L-1的CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,所得滴定曲线如图所示.下列说法一定正确的是( )| A. | A点的pH为1 | |
| B. | B点时:2c(H+)+c(CH3COOH)═2c(OH-)+c(CH3COO-) | |
| C. | 在A→B之间:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | C点时:c(H+)+c(Na+)═c(OH-)+c(CH3COO-) |
| A. | 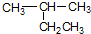 2-乙基丙烷 2-乙基丙烷 | B. | (CH3CH2)2CHCH3 3-甲基戊烷 | ||
| C. | 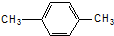 间二甲苯 间二甲苯 | D. | 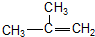 2-甲基-2-丙烯 2-甲基-2-丙烯 |
| A. | CHCl3 | B. | CH3CH2Br | C. | CH3CH2OH | D. | CH2BrCH2CH2OH |
| A. | 393.5kJ | B. | 983.75KJ | C. | 1075.5kJ | D. | 1185.5KJ |