题目内容
【题目】下列描述中正确的是( )
A. CS2为V形的极性分子 B. ClO3﹣的空间构型为平面三角形
C. SiF4和SO32﹣的中心原子均为sp2杂化 D. SF6中有6对相同的成键电子对
【答案】D
【解析】A. CS2与CO2分子构型相同,二氧化碳的分子结构为O=C=O,则CS2的结构为S=C=S,属于直线形分子,故A错误;B.ClO3-中Cl的价层电子对数=3+![]() (7+1-2×3)=4,含有一个孤电子对,则离子的空间构型为三角锥形,故B错误;C.SiF4中Si的价层电子对数=4+
(7+1-2×3)=4,含有一个孤电子对,则离子的空间构型为三角锥形,故B错误;C.SiF4中Si的价层电子对数=4+![]() (4-1×4)=4,SO32-中S的价层电子对数=3+
(4-1×4)=4,SO32-中S的价层电子对数=3+![]() (6+2-2×3)=4,所以中心原子均为sp3杂化,故C错误;D.SF6中S-F含有一个成键电子对,所以SF6中含有6个S-F键,则分子中有6对完全相同的成键电子对,故D正确;故选D。
(6+2-2×3)=4,所以中心原子均为sp3杂化,故C错误;D.SF6中S-F含有一个成键电子对,所以SF6中含有6个S-F键,则分子中有6对完全相同的成键电子对,故D正确;故选D。

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案【题目】周期表里的四种短周期主族元素的相对位置如下所示。已知它们的原子序数总和为38,用元素符号回答以下问题:
m | n | x | |
y |
(1)元素n的原子序数为________;
(2) m、n、x第一电离能的由小到大的顺序:电负性的由大到小的顺序:________。(用元素符号表示)
(3)m、x按照1:2所形成化合物的电子式: ________,分子构型:_____;
(4)用以上任意两种元素写出一个含有极性键的5原子非极性分子式:___
【题目】下列做法中不符合“绿色化学”思想的是
A. 以水性涂料代替油性涂料
B. 以无磷洗涤剂代替含磷洗涤剂
C. 试验后的有毒有害物质应分类收集,统一处理
D. 在通风橱中制取氯气时不用NaOH溶液吸收尾气
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是:
A | B | C | D | |
反应 装置或 图像 |
|
|
|
|
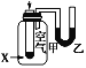
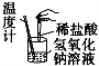
实验现 象或图 像信息 | 反应开始 后,针筒活 塞向右移动 | 反应物总能 量大于生成 物总能量 | 反应开始后, 甲处液面低 于乙处液面 | 温度计的 水银柱不 断上升 |
A. A B. B C. C D. D
【题目】防治雾雾霾天气的主要措施有机动车临时交通管制、工矿企业停业限产、扬尘污染控制等。
(l) PM2.5是环保部门监测空气质量的重要指标。将某PM2.5样本用蒸馏水处理制成待测试样,测得试样中无机离子的种类和平均浓度如下表:
离子种类 | Na+ | NH4+ | SO42- | NO3- |
浓度/(mol/L) | 2.0×l0-6 | 2.8×10-5 | 3.5×10-5 | 6.0×l0-5 |
则试样的pH为____________。
(2)雾霾的主要成分之一是来自汽车尾气的氮氧化物,研究表明CH4可以消除汽车尾气中氮氧化物的污染。
① CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-889.6KJ/mol
② N2(g)+2O2(g)=2NO2(g)ΔH=+67.2KJ/mol
③ 2NO2(g) ![]() N2O4(g) ΔH=-56.9KJ/mol
N2O4(g) ΔH=-56.9KJ/mol
写出甲烷气体催化还原N2O4气体生成稳定的单质气体、二氧化碳气体和液态水的热化学方程式:_____。
(3)一定条件下,以CO 和H2合成清洁能源CH3OH,其热化学方程式为CO(g) + 2H2(g) ![]() CH3OH (g) ΔH,CO的平衡转化率与温度、压强的关系如图所示:
CH3OH (g) ΔH,CO的平衡转化率与温度、压强的关系如图所示:
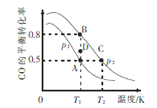
①该可逆反应的ΔH_____0(填“>”“<”“=”)。A,B, C三点对应的平衡常数KA、KB、KC的大小关系是_________。压强:p1_______p2(填“>”“<”“=”)。在T1条件下,由D点到B点过程中,正、逆反应速率之间的关系:v正________v逆(填“>”“<”“=”)。
②若在恒温恒容条件下进行上述反应,能表示该可逆反应达到平衡状态的是__________(填字母)
A. CO的体积分数保持不变
B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内消耗CO的浓度等于生成CH3OH的浓度
③向恒压密闭容器中充入2mol CO和4mol H2,在p2、T2条件下达到平衡状态C点,此时容器容积为2L,则在该条件下反应的平街常数K为______________。