题目内容
7.下列变化需克服相同类型作用力的是( )| A. | 水和液氨的气化 | B. | 硅和C60的熔化 | ||
| C. | AlCl3和NaCl溶于水 | D. | 溴和汞的气化 |
分析 首先判断晶体的类型以及粒子间作用力类型,分子晶体中存在分子间作用力,离子晶体中存在离子键,原子晶体中存在共价键,金属晶体中存在金属键,根据晶体类型分析解答.
解答 解:A.水和氨气都为共价化合物,且存在氢键,水和液氨的气化过程克服氢键,故A正确;
B.硅属于原子晶体,C60属于分子晶体,熔化时分别破坏共价键和分子间作用力,故B错误;
C.氯化铝溶于水破坏共价键,氯化钠溶解破坏离子键,故C错误;
D.溴气化破坏分子间作用力,汞气化破坏金属键,故D错误.
故选A.
点评 本题考查晶体的类型和微粒间作用力的判断,题目难度不大,注意物质发生变化时粒子间作用力的变化.

练习册系列答案
相关题目
4.L一多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下: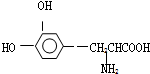 这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
 这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )| A. | 该有机物可看作氨基酸,也可看作是酚类物质 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 分子中至少有7个碳原子在同一平面内 | |
| D. | 既能与溴水发生取代反应,又能与溴水发生加成反应 |
2.检验SO2中是否混有CO2气体,可采用的方法是( )
| A. | 通过品红溶液,若品红溶液褪色,则说明混有CO2气体 | |
| B. | 通过澄清石灰水,若变混浊,则说明混有CO2气体 | |
| C. | 先通过足量NaOH溶液,再通过澄清石灰水,若变混浊,则说明混有CO2气体 | |
| D. | 先通过足量KMnO4溶液(具有强氧化性),再通过澄清石灰水,若变混浊,则说明混有CO2气体 |
12.下列离子在酸性溶液中能大量共存的是( )
| A. | Fe3+、NH4+、SCN-、Cl- | B. | Na+、K+、NO3-、SO42- | ||
| C. | Fe2+、K+、Na+、NO3- | D. | Fe2+、NH4+、Cl-、OH- |
19.下列各组物质中,按熔点由低到高排列正确的是( )
| A. | SiO2、NaCl、CO2 | B. | HF、HCl、HBr | C. | NaCl、KCl、RbCl | D. | Na、Mg、Al |
16.下列有关晶体的叙述中不正确的是( )
| A. | 在晶体中只要有阴离子就一定有阳离子 | |
| B. | 1mol SiO2晶体中含2mol Si-O键 | |
| C. | 干冰晶体中每个CO2分子周围紧邻12个CO2分子 | |
| D. | 金刚石晶体中的最小环由6个碳原子构成 |
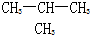 D.甲烷和庚烷
D.甲烷和庚烷