题目内容
(1)某学生欲用11.9 mol·L-1的浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。该学生需要量取________mL浓盐酸进行配制。(保留小数点后1位)
(2)容量瓶是配制溶液的必需仪器。下列关于容量瓶及其使用方法的叙述,错误的是
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液
③容量瓶可以用来加热
④不能用容量瓶长期贮存配制好的溶液
⑤可以用500mL容量瓶配制250mL溶液
⑥容量瓶上标有的是温度 、容量 、刻度线
a.① ③ b.① ④ c.③ ⑤ d.⑤ ⑥
(3)① 该同学用配制的0.400 mol·L-1的盐酸,中和含0.4 g NaOH的NaOH溶液,则该同学需取________mL盐酸。
② 假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是________。
a.浓盐酸挥发,浓度不足
b.配制溶液时,未洗涤烧杯
c.配制溶液时,俯视容量瓶刻度线
d.加水时超过刻度线,用胶头滴管吸出
(2)容量瓶是配制溶液的必需仪器。下列关于容量瓶及其使用方法的叙述,错误的是
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液
③容量瓶可以用来加热
④不能用容量瓶长期贮存配制好的溶液
⑤可以用500mL容量瓶配制250mL溶液
⑥容量瓶上标有的是温度 、容量 、刻度线
a.① ③ b.① ④ c.③ ⑤ d.⑤ ⑥
(3)① 该同学用配制的0.400 mol·L-1的盐酸,中和含0.4 g NaOH的NaOH溶液,则该同学需取________mL盐酸。
② 假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是________。
a.浓盐酸挥发,浓度不足
b.配制溶液时,未洗涤烧杯
c.配制溶液时,俯视容量瓶刻度线
d.加水时超过刻度线,用胶头滴管吸出
(1)16.8(2分)
(2)c(2分)
(3)①25(2分) ②c(2分)
(2)c(2分)
(3)①25(2分) ②c(2分)
试题分析:(1)设需要浓盐酸的体积为V,则11.9 mol·L-1×V="0.5L×0.400" mol·L-1,可得V=0.0168L=16.8mL。
(2)①容量瓶是配制一定体积一定物质的量浓度溶液的专用仪器,正确;②使用前要先检查容量瓶是否漏液,不漏水才能使用,正确;③容量瓶不能加热,错误;④容量瓶是配制溶液的仪器,不能长期贮存配制好的溶液,正确;⑤ 500mL容量瓶只能用来配制500mL溶液,错误;⑥容量瓶上标有的是温度 、容量 、刻度线,正确;故答案为c。
(3)①设需要盐酸的体积为V,则0.400 mol·L-1×V="0.4" g÷40g/mol,可得V=0.025L=25mL。
②所用盐酸的体积比①中所求体积偏小,说明配制溶液的浓度偏高,a、浓盐酸挥发,浓度偏低;b、配制溶液时,未洗涤烧杯,所得溶液浓度偏低;c、配制溶液时,俯视容量瓶刻度线,所得溶液体积偏小,则浓度偏高,正确;d、加水时超过刻度线,浓度偏低。

练习册系列答案
相关题目
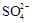 时,先用盐酸酸化,再检验
时,先用盐酸酸化,再检验