题目内容
在某无色溶液,只含有下列8种离子中的一种或几种:Na+、H+、Ag+、Mg2+、Cl-、OH-、HCO3-、NO3-.已知该溶液能跟铝粉反应,且放出的气体只有H2.试回答:
(1)若溶液和铝粉反应后有AlO2-生成,则溶液中一定含有大量的 离子,还可能含有大量的 离子.写出此时放H2的离子方程式 .
(2)若溶液和铝粉反应后有Al3+生成,则溶液中一定含有大量的 离子,原溶液中一定不含有大量的 离子.写出此时放H2的化学方程式 .
(1)若溶液和铝粉反应后有AlO2-生成,则溶液中一定含有大量的
(2)若溶液和铝粉反应后有Al3+生成,则溶液中一定含有大量的
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:跟金属铝反应生成H2的溶液可能为酸溶液,也可能为碱溶液,当生成Al3+时,溶液为酸溶液,当生成AlO2-时,溶液为碱溶液,然后利用离子的共存来分析,并注意离子在水中的颜色.
解答:
解:离子均为无色,与无色透明溶液符合;铝,既能与酸作用产生氢气,也能与碱作用产生氢气,
(1)溶液和铝粉反应后有AlO2-生成,溶液显碱性时,Mg2+、H+、Ag+、HCO3-不能存在,根据溶液不显电性,一定存在阳离子,即阳离子只有Na+,说明原溶液中的阴离子一定含OH-,可能含NO3-、Cl-,则此时放H2的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:Na+、OH-;Cl-、NO3-;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)溶液和铝粉反应后有Al3+生成,溶液显酸性,则HCO3-、OH-不存在,由于硝酸与金属反应一般没有氢气产生,因此也不存在NO3-,
根据溶液不显电性,一定存在阴离子,即溶液中肯定有Cl-,而Ag+可与Cl-生成沉淀,说明原溶液中也不存在Ag+,
即溶液中一定含有大量的H+、Cl-,可能含Na+、Mg2+,一定不存在HCO3-、OH-、NO3-,此时放H2的化学方程式为2Al+6HCl=2AlCl3+3H2↑,
故答案为:H+、Cl-;HCO3-、OH-、NO3-;2Al+6HCl=2AlCl3+3H2↑.
(1)溶液和铝粉反应后有AlO2-生成,溶液显碱性时,Mg2+、H+、Ag+、HCO3-不能存在,根据溶液不显电性,一定存在阳离子,即阳离子只有Na+,说明原溶液中的阴离子一定含OH-,可能含NO3-、Cl-,则此时放H2的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:Na+、OH-;Cl-、NO3-;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)溶液和铝粉反应后有Al3+生成,溶液显酸性,则HCO3-、OH-不存在,由于硝酸与金属反应一般没有氢气产生,因此也不存在NO3-,
根据溶液不显电性,一定存在阴离子,即溶液中肯定有Cl-,而Ag+可与Cl-生成沉淀,说明原溶液中也不存在Ag+,
即溶液中一定含有大量的H+、Cl-,可能含Na+、Mg2+,一定不存在HCO3-、OH-、NO3-,此时放H2的化学方程式为2Al+6HCl=2AlCl3+3H2↑,
故答案为:H+、Cl-;HCO3-、OH-、NO3-;2Al+6HCl=2AlCl3+3H2↑.
点评:本题考查物质的检验及离子的共存问题,明确常见离子之间的反应是解答本题的关键,并注意利用溶液为电中性、溶液的酸碱性等来分析解答即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于热化学反应的描述中正确的是( )
| A、100mL 0.1mol/L盐酸和100mL 0.11mol/L NaOH溶液反应的中和热为△H=-5.73kJ/mol |
| B、1mol乙醇燃烧生成液态水和CO2气体时所放出的热量就是乙醇的燃烧热 |
| C、反应物的总能量高于生成物的总能量时,该反应就一定能发生 |
| D、一个确定的化学反应,其反应热△H 大小与该反应中各物质的状态、反应的条件、反应物的多少都有关系 |
室温下向一定量的稀氨水中加入水稀释后,下列说法正确的是( )
| A、因为稀释,溶液中所有离子的浓度均减小 | ||
B、溶液中
| ||
| C、NH3?H2O的电离程度增大,c(OH-)亦增大 | ||
| D、再加入与氨水等体积等浓度的盐酸,混合液pH=7 |
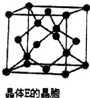 硫元素有多种化合价,可形成多种化合物.
硫元素有多种化合价,可形成多种化合物. (Ⅰ)几种含硅元素的物质之间的相互转化关系如图所示.(注意:在溶液中观察到硅酸沉淀实际上是H4SiO4,H4SiO4在空气中易失水形成H2SiO3)试判断:
(Ⅰ)几种含硅元素的物质之间的相互转化关系如图所示.(注意:在溶液中观察到硅酸沉淀实际上是H4SiO4,H4SiO4在空气中易失水形成H2SiO3)试判断: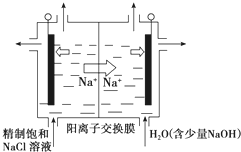 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.