题目内容
【题目】氧是地壳中含量最多的元素,氮是空气中含量最多的元素。
(1)H2O中的O-H键、分子间的范德华力和氢键由强到弱的顺序依次为____>___>___。
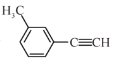
(2)![]() 的沸点高于
的沸点高于 ,其原因是____。
,其原因是____。
(3)O、S、Se都属于第ⅤIA族元素,形成简单氢化物的沸点由高到低的顺序为____>____>____(填分子式)。
(4)如图1表示某种含氮有机化合物的结构简式,其分子内4个氮原子分别位于正四面体的4个顶点(见图2)。分子内存在空腔,能嵌入某种离子或分子并形成4个氢键予以识别。
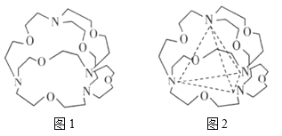
下列分子或离子中,能被该有机化合物识别的是____(填标号)。
A.CF4 B.NH4+ C.CH4 D.H2O
【答案】O-H键 氢键 分子间的范德华力 ![]() 形成分子内氢键,而
形成分子内氢键,而![]() 形成分子间氢键,分子间氢键使分子间作用力增大 H2O H2Se H2S B
形成分子间氢键,分子间氢键使分子间作用力增大 H2O H2Se H2S B
【解析】
(1)氢键键能介于化学键和分子间作用力之间,化学键键能最大,所以H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、范德华力;
(2)含分子间氢键的物质的沸点大于分子内氢键物质的沸点,![]() 形成分子内氢键,而
形成分子内氢键,而![]() 形成分子间氢键,分子间氢键使分子间作用力增大;
形成分子间氢键,分子间氢键使分子间作用力增大;
(3)O、S、Se同主族,其简单氢化物分别为H2O、H2S、H2Se,其中H2O分子之间存在氢键,氢键作用力大于范德华力,导致水的沸点异常的高,对于H2S和H2Se,则是范德华力主导,相对分子质量越高,沸点越高,因此沸点高低顺序为:H2O>H2Se>H2S;
(4)F、O、N电负性很大,与H元素形成的微粒之间可以形成氢键,正四面体顶点N原子与嵌入空腔的微粒形成4个氢键,该微粒应含有4个H原子,C元素不能形成氢键,所以选项中只有NH4+ 符合,故答案为B。

练习册系列答案
相关题目