题目内容
【题目】下列分子结构图中的大黑点表示原子序数小于10的元素的“原子实”(指原子除去最外层电子的剩余部分),小黑点表示没形成共价键的最外层电子,短线表示共价键。其中分子结构图与化学式关系错误的是
A. ![]() (C3H4O)B.
(C3H4O)B. ![]() (HCN)
(HCN)
C. ![]() (NH3)D.
(NH3)D. ![]() (BF3)
(BF3)
【答案】A
【解析】
A、这个分子应该是CO(NH2)2,根据图形可以判断出原子最外层电子数,再根据1~10号原子结构就可以知道这些原子是C、H、N、O,再根据他们的数量就可以推断出该式子代表的物质是尿素,其结构式为![]() ,A错误;
,A错误;
B、从B来看,最左边的原子只形成一个共价键,其最外层只有1个电子,为H,中间原子形成4个共价键,则其最外层有4个电子,在1~10号元素中只有C;最右边原子除形成三个共价键外,还有2个电子剩余,则其最外层有5个电子,在1~10号元素中只有N,所以B的化学式为HCN,B正确;
C、从A来看,上方原子除形成三个共价键外,还有2个电子剩余,则其最外层有5个电子,在1~10号元素中只有N,下方3原子各只形成一个共价键,其最外层只有1个电子,为H,所以A的化学式为NH3,C正确;
D、中间原子只形成三个共价键外,则最外层电子数为3,在1~10号元素中只有B,其它三个原子相同,除形成一个共价键外,还有6个电子剩余,则其最外层有7个电子,在1~10号元素中只有F,所以B的化学式为BF3,D正确;
答案选A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g/100 mL)。
Ⅰ.实验步骤:配制待测白醋溶液,用酸式滴定管量取10.00 mL食用白醋,在烧杯中用水稀释后转移到100 mL容量瓶中定容,摇匀即得待测白醋溶液。量取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
(1)读取盛装0.1000 mol/L NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________ mL。
![]()
(2)滴定。判断滴定终点的现象是________________________________,达到滴定终点,停止滴定,并记录NaOH溶液的最终读数。重复滴定3次。
Ⅱ.实验记录:
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(3)某同学在处理数据时计算得:平均消耗的NaOH溶液的体积V=(15.95+15.00+15.05+14.95)/4=15.24 mL。指出他的计算的不合理之处:_________________。
(4)按正确数据处理,得出c(市售白醋)=_______mol·L-1,市售白醋总酸量=____g·100mL-1。
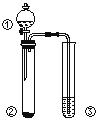
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性: C>Si | |
B | 食盐水 | 电石 | 溴水 | 乙炔可与溴发生加成反应 | |
C | 浓硝酸 | Al | NaOH溶液 | 铝和浓硝酸反应可生成NO2 | |
D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | SO2具有还原性 |
A. A B. B C. C D. D