题目内容
【题目】Ⅰ.用化学用语回答下列问题:
(1)写出![]() 的电子式_______________;
的电子式_______________;
(2)用电子式表示二氧化碳分子的形成过程___________________.
Ⅱ.下列物质:![]()
(3)含有极性键和非极性键的是_____________(填序号,下同);
(4)含有极性键的离子化合物是________________;
Ⅲ.下列物质:![]()
(5)互为同位素的是___________(填序号,下同);
(6)互为同素异形体的是__________________.
(7)氢的三种原子![]() 与氯的两种原子
与氯的两种原子![]()
![]() 相互结合为氯化氢,可得分子中相对分子质量不同的有_______种.
相互结合为氯化氢,可得分子中相对分子质量不同的有_______种.
【答案】![]()
![]() ②⑤①③5
②⑤①③5
【解析】
Ⅰ.(1)氢氧化钠属于离子化合物,有钠离子和氢氧根离子构成,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)二氧化碳属于共价化合物,分子中C原子与O原子之间形成2对共用电子对,所有原子的最外层都满足8电子结构,用C原子、O原子的电子式表示其形成为:![]() ,故答案为:
,故答案为:![]() ;
;
Ⅱ.![]() 中只含有非极性键;
中只含有非极性键;![]() 中含有H-O极性键和O-O非极性键;
中含有H-O极性键和O-O非极性键;![]() 中只含有极性键;
中只含有极性键;![]() 中含有离子键;
中含有离子键;![]() 中含有离子键和极性共价键;
中含有离子键和极性共价键;
(3)含有极性键和非极性键的是![]() ,故答案为:
,故答案为:![]() ;
;
(4)含有极性键的离子化合物是⑤,故答案为:⑤;
Ⅲ. (5)①1H、2H、3H是氢元素的不同核素,互为同位素,故答案为:①;
(6)③O2、O3,是氧元素的不同单质,为同素异形体,故答案为:③;
(7)氢原子有三种同位素1H、2H、3H,氯原子有两种的同位素35Cl、37Cl,故氯化氢分子可能为:1H35Cl、1H37Cl、2H35Cl、2H37Cl、3H35Cl、3H37Cl,则形成的氯化氢分子的种类有6种,分子中相对分子质量分别为:36、38、37、39、38、40,不同的有5种,故答案为:5。

 名校课堂系列答案
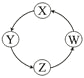
名校课堂系列答案【题目】下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①②③ B. ①③④ C. ②③ D. ①④