题目内容
Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2++2H2O?Fe(OH)2+2H+,往该溶液中滴加盐酸,发生的变化是( )
| A、平衡向逆反应方向移动 |
| B、平衡不移动 |
| C、溶液由浅绿色变成黄色 |
| D、溶液由浅绿色变为深绿色 |
考点:化学平衡移动原理
专题:
分析:根据离子浓度对盐类水解平衡的影响分析解答,注意二价铁离子有还原性,硝酸有强氧化性,亚铁离子和硝酸能发生氧化还原反应生成三价铁离子.
解答:
解:加入盐酸时,氢离子浓度增大,平衡逆向移动,酸性条件下亚铁离子被硝酸根离子氧化生成铁离子,导致平衡逆向移动,所以溶液由浅绿色变成黄色,故选AC.
点评:本题考查了影响盐类水解,注意酸性条件下,硝酸根离子和亚铁离子能发生氧化还原反应而使亚铁离子生成铁离子,属于易错题.

练习册系列答案
相关题目
既可以鉴别甲烷和乙烯,又可以用来除去甲烷中的乙烯的方法是( )
| A、混合气体通过盛水的洗气瓶 |
| B、混合气体通过装有过量溴水的洗气瓶 |
| C、混合气体和过量氢气混合 |
| D、混合气体通过酸性高锰酸钾溶液 |
将固体NH4I置于密闭容器中,在某温度下,发生下列反应:
NH4I(s)?NH3(g)+HI(g);2HI(g)?H2(g)+I2(g)
当达化学平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则容器中NH3、HI、I2的物质的量之比是( )
NH4I(s)?NH3(g)+HI(g);2HI(g)?H2(g)+I2(g)
当达化学平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则容器中NH3、HI、I2的物质的量之比是( )
| A、8:8:1 |
| B、10:8:1 |
| C、2:2:1 |
| D、3:2:1 |
下列物质组合中,既能和酸反应又能和碱反应的化合物是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤SiO2.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤SiO2.
| A、①②③⑤ | B、①②③④⑤ |
| C、①③⑤ | D、②③④ |
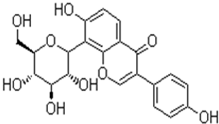 葛根素是由葛根提取制成,主要化学成份为皂苷类化合物葛根黄酮,具有提高免疫,增强心肌收缩力,降低血压,抗血小板聚集等作用.葛根素分子的结构简式如图,下列有关说法正确的是( )
葛根素是由葛根提取制成,主要化学成份为皂苷类化合物葛根黄酮,具有提高免疫,增强心肌收缩力,降低血压,抗血小板聚集等作用.葛根素分子的结构简式如图,下列有关说法正确的是( )| A、该物质一定条件下能发生消去、加成、水解等反应 |
| B、葛根素的分子式为C21H22O9 |
| C、该物质一个分子中含有5个手性碳原子 |
| D、1mol该物质一定条件下最多能消耗H2 8mol,Br2 4mol |
所有原子都在一条直线上的分子是( )
| A、C2H4 |
| B、CO2 |
| C、C3H4 |
| D、CH4 |
区别SO2和CO2气体可选用( )
| A、通入澄清石灰水中 |
| B、通入品红溶液中 |
| C、用带火星的木条检验 |
| D、通入石蕊试液中 |
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )

| A、X是正极,Y是负极,CuSO4溶液的pH逐渐减小 |
| B、X是正极,Y是负极,CuSO4溶液的pH保持不变 |
| C、X是负极,Y是正极,CuSO4溶液的pH逐渐减小 |
| D、X是负极,Y是正极,CuSO4溶液的pH保持不变 |
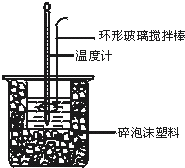 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: