题目内容
下列叙述正确的是
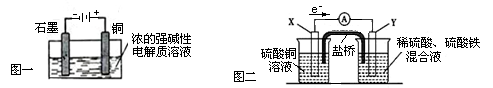

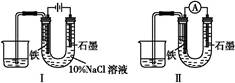
| A.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图一所示,石墨电极上产生氢气,铜电极发生氧化反应 |
| B.图一所示当有0.1mol电子转移时,有0.1molCu2O生成 |
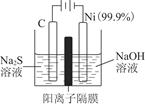
| C.图二装置中发生:Cu+2Fe3+ = Cu2++2Fe2+,X极是负极,Y极材料可以是铜 |
| D.如图二,盐桥的作用是传递电荷以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中 |
A
试题分析:图一为电解池,电解质溶液为强碱性溶液,石墨电极与电源负极相连为阴极,发生还原反应:2H2O + 2e- = H2↑+ 2OH-,铜电极与电源正极相连为阳极,发生氧化反应:2Cu – 2e- + 2OH- = Cu2O + H2O ,电解总反应为:2Cu+H2OCu2O+H2↑。由此可知A选项正确。根据电解总反应可知,当有0.2mol电子转移时,才有0.1molCu2O生成, B选项不正确。图二装置为原电池,根据图中给出的电子流向,可以判断X极是电池的负极,Y极是电池的正极;根据装置中发生的反应:Cu+2Fe3+ = Cu2++2Fe2+,可知X极为负极,失电子,发生氧化反应,即Cu-2e- = Cu2+,所以X极的材料应该是铜。依据原电池的形成条件,Y极材料应该是活动性比铜弱的金属或石墨等材料,故C选项不正确。盐桥的作用①盐桥中离子的定向迁移构成了电流通路,从而沟通内电路,形成闭合回路,保障了电子通过外电路从电池负极到正极的不断转移,使原电池不断产生电流;②平衡电荷,盐桥可使由它连接的两个半电池中的溶液保持电中性,同时又能阻止反应物直接接触。所以,Fe3+是不能经过盐桥进入左侧烧杯中,故D选项不正确。

练习册系列答案
相关题目
 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )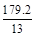 L
L