题目内容
【题目】固体氧化物燃料电池是一种新型的燃料电池,它是以固体氧化钇(Y2O3)、氧化锆(ZrO2)为解质,这种电解质在高温熔融状态下允许氧离子(O2-)在其间通过。某甲醇燃料电池的工作原理如右图所示,两个多孔电极均不参与电极反应。下列有关该燃料电池的说法错误的是(已知每摩尔电子所携带的电量为9.65×104C/mol)
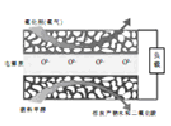
A. 该燃料电池的负极反应式为CH3OH-6e-+3O2-=CO2↑+2H2O
B. 若有16g甲醇发生反应,该电池理论上提供的电量最多为2.895×105C
C. 氧气在负极发生还原反应
D. O2-在电解质中的移动方向为:正极![]() 负极
负极
【答案】C
【解析】A.甲醇具有还原性,为原电池的负极,电极反应式为CH3OH-6e-+3O2-=CO2↑+2H2O,A正确;B. 若有16g甲醇即0.5mol甲醇发生反应,转移电子是3mol,则该电池理论上提供的电量最多为9.65×104C/mol×3mol=2.895×105C,B正确;C.通入氧气的一极为原电池的正极,发生还原反应,C错误;D.原电池中阴离子向负极移动,则O2-在电解质中的移动方向为:正极→负极,D正确,答案选C。

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目