题目内容
7.化学方程式可简明地体现元素及其化合物的性质.已知:氧化还原反应:
2FeCl3+2HI═2FeCl2+I2+2HCl;
2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O
2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI;
3I2+6KOH═5KI+KIO3+3H2O
复分解反应:
2HSCN+K2CO3═2KSCN+CO2↑+H2O;
KCN+CO2+H2O═HCN+KHCO3
热分解反应:4NaClO$\frac{\underline{\;\;△\;\;}}{\;}$3NaCl+NaClO4;NaClO4$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2O2↑
下列说法不正确是:( )
| A. | 酸性(吸水溶液):HSCN>H2CO3>HCN | B. | 还原性(碱性溶液):Fe(OH)2>I->KIO3 | ||
| C. | 热稳定性:NaCl>NaClO4>NaClO | D. | 氧化性(酸性溶液):I2>FeCl3>Co(OH)3 |
分析 A.2HSCN+K2CO3═2KSCN+CO2↑+H2O、KCN+CO2+H2O═HCN+KHCO3均为强酸制取弱酸的反应;
B.2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI、3I2+6KOH═5KI+KIO3+3H2O中还原剂的还原性大于还原产物的还原性;
C.由4NaClO$\frac{\underline{\;\;△\;\;}}{\;}$3NaCl+NaClO4、NaClO4$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2O2↑,可知分解为更稳定的化合物;
D.2FeCl3+2HI═2FeCl2+I2+2HCl、2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中氧化剂的氧化性大于氧化产物的氧化性.
解答 解:A.2HSCN+K2CO3═2KSCN+CO2↑+H2O、KCN+CO2+H2O═HCN+KHCO3均为强酸制取弱酸的反应,可知酸性为HSCN>H2CO3>HCN,故A正确;
B.2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI、3I2+6KOH═5KI+KIO3+3H2O中还原剂的还原性大于还原产物的还原性,则还原性为Fe(OH)2>I->KIO3,故B正确;
C.由4NaClO$\frac{\underline{\;\;△\;\;}}{\;}$3NaCl+NaClO4、NaClO4$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2O2↑,可知分解为更稳定的化合物,则热稳定性为NaCl>NaClO4>NaClO,故C正确;
D.2FeCl3+2HI═2FeCl2+I2+2HCl、2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中氧化剂的氧化性大于氧化产物的氧化性,则氧化性为Co(OH)3>Cl2>FeCl3>I2,故D错误;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握氧化还原反应中元素的化合价变化及反应原理、规律性知识的应用为解答的关键,侧重分析与应用能力的考查,题目难度不大.

| Na2O2/mol | NaHCO3/mol | 气体成分 | |
| A | 1 | 2 | Na2CO3 |
| B | 1.5 | 2 | Na2O2 Na2CO3 |
| C | 2 | 1 | Na2CO3、NaOH、Na2O2 |
| D | 3 | 2 | NaOH、Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 碳酸钾 | B. | 硫酸钾 | C. | 碳酸钠 | D. | 硫酸钠 |
| A. | 18g水中含有的原子数为2NA | |
| B. | 11.2L O2一定含有NA个原子 | |
| C. | 标准状况下,NA个水分子所占体积为22.4L | |
| D. | NA个氧分子和NA个氢分子的质量比等于16:1 |
| A. | 反应中KMnO4被氧化 | |
| B. | 氧化产物与还原产物的物质的量之比为5﹕2 | |
| C. | 每生成0.5 mol Cl2时,反应中转移的电子为2 mol | |
| D. | 氧化剂和还原剂的比是1:8 |
| A. | H2SO4═2H++SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | KClO3═K++Cl-+3O2- | D. | NaHSO4═Na++HSO4- |
| A. | 任何化学反应,只要化学反应的速率很快,理论上都能设计成原电池 | |
| B. | 中和反应一定是放热反应 | |
| C. | 化学反应的速率可通过改变条件而改变 | |
| D. | 化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
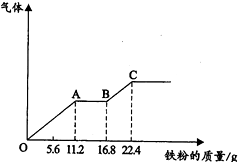 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁质量增加的变化如图所示.反应前后溶液体积不发生变化.
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁质量增加的变化如图所示.反应前后溶液体积不发生变化.