题目内容
下列说法一定正确的是( )
| A.氯碱工业中若阳极产生0.1mol氯气则通过溶液的电子的物质的量为0.2mol |
| B.1L 1mol/LNa2CO3溶液中阴离子和阳离子的总数为3×6.02×1023 |
C.当碳酸溶液的PH增大1时,溶液中 可能增大也可能减小 可能增大也可能减小 |
| D.乙烯和苯分子中都存在碳碳双键,都能发生加成反应 |
C
电化学中电子只能在导线中传递,而不能在溶液中,A不正确。碳酸钠水解显碱性,应用消耗1mol碳酸钠产生1mol碳酸氢钠和1mol氢氧化钠,所以溶液中阴离子和阳离子的总数大于3×6.02×1023,B不正确。碳酸的酸性增强,其电离平衡可能被抑制,也可能被促进,C增强。苯分子中不存在碳碳双键,D不正确,答案选C。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
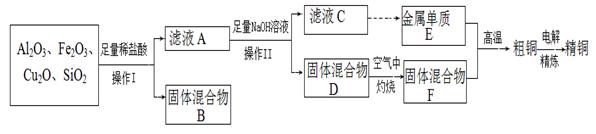
 已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
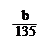 mol
mol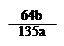 ×100℅
×100℅ 

 氢气及氢氧化钠反应
氢气及氢氧化钠反应