题目内容
【题目】工业上处理含Cr2O![]() 的酸性工业废水用以下方法:
的酸性工业废水用以下方法:
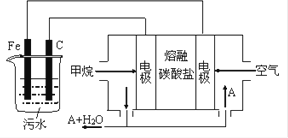
①往工业废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀生成;③过滤回收沉淀,废水达排放标准。试回答:
(1)电解时的电极反应,阳极 , 阴极。
(2)写出Cr2O![]() 转变成Cr3+的离子反应方程式。
转变成Cr3+的离子反应方程式。
(3)电解过程中Cr(OH)3和Fe(OH)3沉淀是怎样产生的?。
(4)能否将Fe电极改成石墨电极?为什么?
【答案】
(1)Fe-2e-=Fe2+;2H++2e-=H2↑
(2)6Fe2++Cr2O![]() +14H+=6Fe3++2Cr3++7H2O
+14H+=6Fe3++2Cr3++7H2O
(3)Fe3+、Cr3+与溶液中OH-形成Fe(OH)3、Cr(OH)3沉淀
(4)
不能用石墨电极代替Fe电极。因为Fe电极在电解过程中产生还原性的Fe2+,将溶液中Cr2O![]() 还原为Cr3+而除去,若改用石墨电极,不能产生还原性微粒
还原为Cr3+而除去,若改用石墨电极,不能产生还原性微粒
【解析】(1)铁电极作阳极,铁被氧化而溶解:Fe-2e-=Fe2+ , 阴极上溶液中氢离子放电生成氢气:2H++2e-=H2↑;(2)阳极生成的Fe2+与含Cr2O![]() 的酸性工业废水发生氧化还原反应,离子方程式为6Fe2++Cr2O
的酸性工业废水发生氧化还原反应,离子方程式为6Fe2++Cr2O![]() +14H+=6Fe3++2Cr3++7H2O;(3)由于阴极H+放电,破坏了水的电离平衡,H2O=H++OH- , 溶液中OH-浓度逐渐增大并向阳极移动,与Fe3+、Cr3+形成Fe(OH)3、Cr(OH)3沉淀;(4)不能用石墨电极代替Fe电极,因为Fe电极在电解过程中产生还原性的Fe2+ , 将溶液中Cr2O
+14H+=6Fe3++2Cr3++7H2O;(3)由于阴极H+放电,破坏了水的电离平衡,H2O=H++OH- , 溶液中OH-浓度逐渐增大并向阳极移动,与Fe3+、Cr3+形成Fe(OH)3、Cr(OH)3沉淀;(4)不能用石墨电极代替Fe电极,因为Fe电极在电解过程中产生还原性的Fe2+ , 将溶液中Cr2O![]() 还原为Cr3+而除去,若改用石墨电极,不能产生还原性微粒。
还原为Cr3+而除去,若改用石墨电极,不能产生还原性微粒。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案
相关题目