题目内容
在试管中注入某红色溶液,将试管微热,溶液颜色逐渐变浅,则原溶液可能是( )
①滴有石蕊的NH4Cl溶液 ②滴有酚酞的氨水溶液
③滴有酚酞的饱和氢氧化钙溶液 ④滴有酚酞的CH3COONa溶液.
①滴有石蕊的NH4Cl溶液 ②滴有酚酞的氨水溶液
③滴有酚酞的饱和氢氧化钙溶液 ④滴有酚酞的CH3COONa溶液.
| A、①④ | B、②③ | C、①③ | D、②④ |
分析:①氯化铵溶液水解呈酸性,指示剂石蕊变红色,加热促进水解;
②氨水是弱碱溶液电离出氢氧根离子遇到酚酞变红,加热一水合氨分解挥发氨气,氢氧根离子减少;
③氢氧化钙溶解度随温度升高减小,饱和氢氧化钙溶液温度升高会析出氢氧化钙晶体;
④CH3COONa溶液水解显碱性遇到酚酞变红,加热促进水解;
②氨水是弱碱溶液电离出氢氧根离子遇到酚酞变红,加热一水合氨分解挥发氨气,氢氧根离子减少;
③氢氧化钙溶解度随温度升高减小,饱和氢氧化钙溶液温度升高会析出氢氧化钙晶体;
④CH3COONa溶液水解显碱性遇到酚酞变红,加热促进水解;
解答:解:①加热有利于NH4+的水解,NH4+水解呈酸性,所以加热会使颜色变深,故①不符合;
②因为无色酚酞试液遇氨水显红色,由于氨水具有挥发性,所以当加热时,氨水中的氨分子挥发,氢氧根离子浓度减少,溶液的红色变浅,故②符合;
③滴有酚酞的饱和氢氧化钙溶液呈红色,氢氧化钙的溶解度随温度的升高而降低,加热后,溶解在溶液中的氢氧化钙减少,溶液中OH-降低,颜色变浅,故③符合;
④滴有酚酞的CH3COONa溶液,醋酸根离子水解呈碱性CH3COO-+H2O?CH3COOH+OH-;水解是吸热反应,加热促进水解,氢氧根离子浓度增大,红色变深,故④不符合;
综上所述:②③符合
故选B.
②因为无色酚酞试液遇氨水显红色,由于氨水具有挥发性,所以当加热时,氨水中的氨分子挥发,氢氧根离子浓度减少,溶液的红色变浅,故②符合;
③滴有酚酞的饱和氢氧化钙溶液呈红色,氢氧化钙的溶解度随温度的升高而降低,加热后,溶解在溶液中的氢氧化钙减少,溶液中OH-降低,颜色变浅,故③符合;
④滴有酚酞的CH3COONa溶液,醋酸根离子水解呈碱性CH3COO-+H2O?CH3COOH+OH-;水解是吸热反应,加热促进水解,氢氧根离子浓度增大,红色变深,故④不符合;
综上所述:②③符合
故选B.
点评:本题考查了元素化合物的性质应用,主要考查盐类水解平衡的影响因素分析,指示剂的颜色变化.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
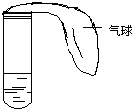 某学生课外活动小组利用右图所示装置分别做如下实验:
某学生课外活动小组利用右图所示装置分别做如下实验: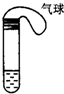 I向一金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,解释上述变化的实验现象:
I向一金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,解释上述变化的实验现象: