题目内容
下列各组微粒中,各电子层电子数均达到2n2个的是
A . F—和S2- B. Ne和Cl— C Ne和 Ar D. H —和Na +
A . F—和S2- B. Ne和Cl— C Ne和 Ar D. H —和Na +
D
当n=1时,电子层只有一个,第一电子层也是其最外电子层,最多排2个电子;
当n=2时,最外层是第二电子层,最多排8个电子,各电子层能达到2n2个电子,所以只要核外电子数是10个的原子或离子都可.
当n=3时,最外层是第三电子层,最多排8个电子,不是各电子层能达到2n2个电子,所以舍去.
所以符合条件的是有2个电子或10个电子的原子或离子.
S2-不符合条件,故A错误; Cl-不符合条件,故B错误;Ar不符合条件,故C错误; D、HA-、Na+各个电子层电子数都达到2n2个,正确,故选C.
点评:本题考查了原子核外电子的排布,难度不大,注意每个电子层上最多排2n2个,但还要符合最外层电子数不大于8个,次外层不大于18个,倒数第三层不大于32个的规则.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 ,熔成小球,做不定向运动,随之消失,溶液变成红色。
,熔成小球,做不定向运动,随之消失,溶液变成红色。 2
2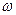

 )、钚-239(
)、钚-239( )和钚-240(
)和钚-240( ),“表明了事故的重大性和严重性”。3月30日,在我国沿海和内地的部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素碘-131(
),“表明了事故的重大性和严重性”。3月30日,在我国沿海和内地的部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素碘-131( ),其对公众可能产生的附加辐射剂量小于岩石、土壤、建筑物、食物、太阳等自然辐射源的天然本底辐射剂量的十万分之一,对环境和公众健康不会产生影响,无需采取任何防护措施。下列关于钚元素和碘元素的说法正确的是:
),其对公众可能产生的附加辐射剂量小于岩石、土壤、建筑物、食物、太阳等自然辐射源的天然本底辐射剂量的十万分之一,对环境和公众健康不会产生影响,无需采取任何防护措施。下列关于钚元素和碘元素的说法正确的是: