题目内容
某氧化还原反应中包含下列物质:Na3AsO4、H2O2、Na2SO4、As2S3、H2O和NaOH。已知H2O2是唯一的氧化剂,水是生成物。下列有关说法正确的是
| A.NaOH是生成物 |
| B.反应中As2S与H2O2的物质的量之比为1: 14 |
| C.配平后化学计量数最大的物质是H2O2 |
| D.生成l mol H2O时转移1.2 mol电子 |
B
Na3AsO4、H2O2、Na2SO4、As2S3、H2O和NaOH中,H2O2是唯一的氧化剂,则As2S3是还原剂,该反应的化学方程式为:
14H2O2 + As2S3 + 12NaOH ===== 2Na3AsO4 + 3Na2SO4 + 20H2O
在该方程式中每生成20 mol H2O转移的电子数为28 mol,则生成l mol H2O时转移1.4 mol电子
14H2O2 + As2S3 + 12NaOH ===== 2Na3AsO4 + 3Na2SO4 + 20H2O
在该方程式中每生成20 mol H2O转移的电子数为28 mol,则生成l mol H2O时转移1.4 mol电子

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
 (2) 3Cl2 + 6NaOH 5NaCl + NaClO3 + 3H2O
(2) 3Cl2 + 6NaOH 5NaCl + NaClO3 + 3H2O
 转变为
转变为 沉淀得以分离。其反应的化学方程式可表示为
沉淀得以分离。其反应的化学方程式可表示为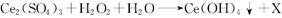 (未配平)。下列对该反应的说法不正确的是
(未配平)。下列对该反应的说法不正确的是
 ,转移电子的物质的量为0. 25 mol
,转移电子的物质的量为0. 25 mol 2Fe+3CO2
2Fe+3CO2 的物质的质量是 g。
的物质的质量是 g。 ,还原剂是 ,氧化产物是 ,还原产物是 ,假如有2.5 molCl2生成,则该反应中电子转移数目为___________________。
,还原剂是 ,氧化产物是 ,还原产物是 ,假如有2.5 molCl2生成,则该反应中电子转移数目为___________________。 (4)测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(4)测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。