题目内容
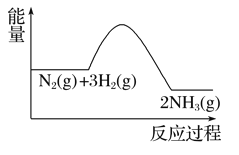
【题目】下列反应过程能量变化如下所示:H2(g)+Cl2(g)===2HCl(g) ΔH
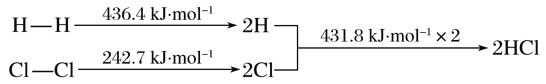
下列说法错误的是( )
A. H—H键比Cl—Cl键稳定
B. 正反应活化能比逆反应活化能高
C. ΔH=-184.5 kJ·mol-1
D. 在相同条件下,1 mol H2(g)和1 mol Cl2(g)分别在点燃和光照条件下反应生成2 mol HCl(g),重新恢复到原来的状态时ΔH相同
【答案】B
【解析】A.因为H2的键能大于Cl2的键能,所以H-H键比Cl-Cl键稳定,故A正确;B.H2(g)+Cl2(g)═2HCl(g)△H<0,说明正反应活化能比逆反应活化能低,故B错误;C.△H=(436.4 kJmol-1+242.7 kJmol-1)-(431.8 kJmol-1)×2=-184.5kJmol-1,故C正确; D.△H与起点和终点有关,与反应的条件无关,故D正确;故选B。

 阅读快车系列答案
阅读快车系列答案【题目】下列说法中,不正确的是
A | B | C | D |
|
|
|
|
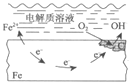
钢铁表面水膜的酸性很弱或呈中性,发生吸氧腐蚀 | 钢铁表面水膜的酸性较强,发生析氢腐蚀 | 将锌板换成铜板对钢闸门保护效果更好 | 钢闸门作为阴极而受到保护 |
A. A B. B C. C D. D
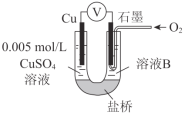
【题目】某小组同学利用原电池装置探究物质的性质。
资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。 |
(1)同学们利用下表中装置进行实验并记录。
装置 | 编号 | 电极A | 溶液B | 操作及现象 |
| Ⅰ | Fe | pH=2的 H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_________。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_________;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是_________。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性的因素。
编号 | 溶液B | 操作及现象 |
Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是_________。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究对O2氧化性的_________影响。
③实验Ⅳ中加入Na2SO4溶液的目的是_________。
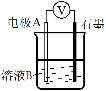
④为达到丁同学的目的,经讨论,同学们认为应改用右图装置对Ⅳ、Ⅴ重复进行实验,其设计意图是_________;重复实验时,记录电压表读数依次为c′、d′,且c′>d′,由此得出的结论是_________。