题目内容
【题目】(1)写出铁与水蒸气在高温下反应方程式___________________________。
(2)常温下,铜在潮湿的空气里会被锈蚀,有关化学方程式为___________________________________。
(3)在呼吸面具中,Na2O2 起反应的化学方程式为____________________________________。当有7.8克Na2O2反应时,放出氧气的质量为____________。
(4)将6.4g的铜片投入到100ml的FeCl3溶液中恰好完全反应,发生的反应离子方程式为______________________________________, FeCl3溶液的物质的量浓度______________。
(5)向FeSO4溶液中滴加NaOH溶液时,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色。写出此变化过程的化学方程式:_________________________________________。
【答案】 3Fe + 4H2O(g)![]() Fe3O4 + 4H2 2Cu + O2 +CO2 + H2O =Cu2(OH)2CO3 2Na2O2 + 2CO2 == 2Na2CO3 + O2 1.6克 2Fe3+ + Cu = 2Fe2+ + Cu2+ 2mol/L FeSO4 + 2NaOH = Fe(OH)2 ↓+ Na2SO4, 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
Fe3O4 + 4H2 2Cu + O2 +CO2 + H2O =Cu2(OH)2CO3 2Na2O2 + 2CO2 == 2Na2CO3 + O2 1.6克 2Fe3+ + Cu = 2Fe2+ + Cu2+ 2mol/L FeSO4 + 2NaOH = Fe(OH)2 ↓+ Na2SO4, 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
【解析】试题分析:(1)铁与水蒸气在高温下反应生成四氧化三铁和氢气;(2)常温下,铜在潮湿的空气里会与氧气、二氧化碳反应生成Cu2(OH)2CO3;(3)在呼吸面具中,Na2O2与二氧化碳反应放出氧气;根据方程式计算7.8克Na2O2反应时,放出氧气的质量;(4)铜片投入FeCl3溶液中生成氯化亚铁和氯化铜;根据反应方程式计算FeCl3溶液的物质的量浓度;(5)FeSO4溶液中滴加NaOH溶液时,生成的白色Fe(OH)2沉淀,Fe(OH)2被氧气氧化为红褐色Fe(OH)3沉淀。
解析:(1)铁与水蒸气在高温下反应生成四氧化三铁和氢气,反应方程式是3Fe + 4H2O(g)![]() Fe3O4 + 4H2 ;(2)常温下,铜在潮湿的空气里会与氧气、二氧化碳反应生成Cu2(OH)2CO3,反应方程式是2Cu + O2 +CO2 + H2O =Cu2(OH)2CO3;(3)在呼吸面具中,Na2O2与二氧化碳反应生成碳酸钠和氧气,反应方程式是2Na2O2 + 2CO2 == 2Na2CO3 + O2;
Fe3O4 + 4H2 ;(2)常温下,铜在潮湿的空气里会与氧气、二氧化碳反应生成Cu2(OH)2CO3,反应方程式是2Cu + O2 +CO2 + H2O =Cu2(OH)2CO3;(3)在呼吸面具中,Na2O2与二氧化碳反应生成碳酸钠和氧气,反应方程式是2Na2O2 + 2CO2 == 2Na2CO3 + O2;
设 7.8克Na2O2反应时,放出氧气的质量为xg

![]() , x=1.6g;
, x=1.6g;
(4)铜片投入FeCl3溶液中生成氯化亚铁和氯化铜,反应离子方程式是2Fe3+ + Cu = 2Fe2+ + Cu2+;设100ml FeCl3溶液中含有FeCl3的物质的量是xmol;
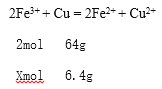
![]() ,x=0.2mol;FeCl3溶液的物质的量浓度为
,x=0.2mol;FeCl3溶液的物质的量浓度为![]() ;(5)FeSO4溶液中滴加NaOH溶液时,生成的白色Fe(OH)2沉淀,反应方程式是FeSO4 + 2NaOH = Fe(OH)2 ↓+ Na2SO4,Fe(OH)2被氧气氧化为红褐色Fe(OH)3沉淀,反应方程式是4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
;(5)FeSO4溶液中滴加NaOH溶液时,生成的白色Fe(OH)2沉淀,反应方程式是FeSO4 + 2NaOH = Fe(OH)2 ↓+ Na2SO4,Fe(OH)2被氧气氧化为红褐色Fe(OH)3沉淀,反应方程式是4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。

 名校课堂系列答案
名校课堂系列答案