题目内容
19.写出下列化学反应方程式:(1)溴乙烷与NaOH的乙醇溶液共热:CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O.
(2)将CO2通入苯酚钠溶液中:
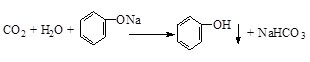 .
.(3)1,3-丁二烯的与Br2的1、4加成反应:
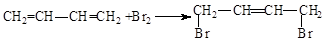 .
.(4)葡萄糖与银氨溶液发生银镜反应:CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{水浴加热}{→}$CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O.
分析 (1)溴乙烷和NaOH的醇溶液加热发生消去反应生成乙烯;
(2)二氧化碳通入苯酚钠中生成苯酚、碳酸氢钠;
(3)1,3-丁二烯和溴发生1,4加成生成1,4-二溴-2-丁烯;
(4)葡萄糖与银氨溶液发生银镜反应生成葡萄糖酸铵、银、氨气和水.
解答 解:(1)溴乙烷和NaOH的醇溶液加热发生消去反应生成乙烯,反应方程式为CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O,故答案为:CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O;
(2)二氧化碳通入苯酚钠中生成苯酚、碳酸氢钠,反应方程式为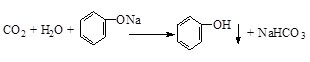 ,
,
故答案为: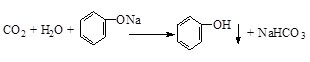 ;
;
(3)1,3-丁二烯和溴发生1,4加成生成1,4-二溴-2-丁烯,反应方程式为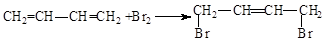 ,
,
故答案为: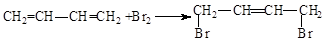 ;
;
(4)葡萄糖与银氨溶液发生银镜反应生成葡萄糖酸铵、银、氨气和水,反应方程式为CH2OH(CHOH)4CHO+2Ag(NH3)2OH $\stackrel{水浴加热}{→}$CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,
故答案为:CH2OH(CHOH)4CHO+2Ag(NH3)2OH $\stackrel{水浴加热}{→}$CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O.
点评 本题考查化学反应方程式的书写,为高频考点,会根据反应物、生成物及反应条件书写方程式,明确官能团及其性质关系,知道断键和成键位置,题目难度不大.

练习册系列答案
相关题目
9.下列叙述正确的是( )
| A. | 最外层有1个电子的元素一定是金属元素 | |
| B. | 除0族元素外,第三周期元素的原子半径不一定比第二周期元素的原子半径大 | |
| C. | 同主族元素从上到下,元素原子得电子能力逐渐减弱,氢化物的稳定性逐渐增强 | |
| D. | 主族元素的原子,最外层电子数少的一定比最外层电子数多的失电子能力强 |
10.冶炼金属一般有下列四种方法:①焦炭法,②水煤气(或H2或CO)法,③活泼金属置换法,④电解法.
四种方法在工业上均有应用,古代有(Ⅰ)火烧孔雀石法炼铜,(Ⅱ)湿法炼铜,现代有(Ⅲ)铝热法炼铬,(Ⅳ)从光卤石(KCl•MgCl2•6H2O)中炼镁,对它们的冶炼方法分析不正确的是( )
四种方法在工业上均有应用,古代有(Ⅰ)火烧孔雀石法炼铜,(Ⅱ)湿法炼铜,现代有(Ⅲ)铝热法炼铬,(Ⅳ)从光卤石(KCl•MgCl2•6H2O)中炼镁,对它们的冶炼方法分析不正确的是( )
| A. | (Ⅰ)用 ① | B. | (Ⅱ)用 ② | C. | (Ⅲ)用 ③ | D. | (Ⅳ)用 ④ |
7.下列关于海水知识的叙述不正确的是( )
| A. | 海水既苦又涩,不能直接利用 | |
| B. | 海水资源的利用包括海水水资源利用和化学资源利用 | |
| C. | 海水中某些金属元素总储量很大,但富集程度却很低 | |
| D. | 海水淡化应同化工生产结合,同能源技术结合 |
14.既可以用来鉴别乙烷与乙烯,又可以用来除去乙烷中乙烯方法是( )
| A. | 通过足量的NaOH溶液 | B. | 通过足量的酸性KMnO4溶液 | ||
| C. | 在Ni催化、加热条件下通入H2 | D. | 通过足量的溴水 |
4.下列叙述不正确的是( )
| A. | 盐析可提纯蛋白质并保持其生理活性 | |
| B. | 油脂水解可得到丙三醇 | |
| C. | 打针时用75%的乙醇溶液消毒是蛋白质变性知识的应用 | |
| D. | 蛋白质、纤维素、油脂、淀粉都是高分子化合物 |
11.下列有机物的同系物中,①乙炔的同系物;②苯的同系物;③饱和的一元醇;④饱和的一元醛;⑤饱和的一元羧酸;⑥饱和的一元醇和饱和的一元羧酸生成的酯.完全燃烧产生的水和二氧化碳的物质的量之比恒定的是( )
| A. | ①④⑤ | B. | ④⑤⑥ | C. | ③④⑥ | D. | ①②④⑤⑥ |
9.某无色透明溶液能与铝作用放出氢气,此溶液中一定能大量共存的离子组是( )
| A. | NO3-、Cu2+、Cl-、NH4+ | B. | K+、CO32-、Ca+、NO3- | ||
| C. | HCO3-、Na+、NO3-、K+ | D. | Cl-、SO42-、Na+、K+ |