题目内容
某小组为研究电化学原理,设计如图装置。下列叙述错误的是
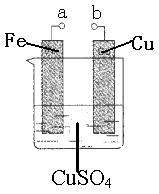

| A.a和b不连接时,铁片质量会增加 |
| B.a和b用导线连接时,正极发生的电极反应为:Cu2++2e-=Cu |
| C.无论a和b是否连接,铁片均被腐蚀 |
| D.a和b分别连接电源正、负极时,Fe电极发生的电极反应为:4OH--4e-=2H2O+O2↑ |
D
试题分析:A、a和b不连接时,铁与硫酸铜发生置换反应生成铜与硫酸亚铁。生成的铜附着在铁片上,因此铁片质量会增加,A正确;B、a和b用导线连接时构成原电池,铁的金属性强于铜,因此铁是负极,铜是正极,则正极发生的电极反应为:Cu2++2e-=Cu,B正确;C、a和b用导线连接时构成原电池,铁的金属性强于铜,因此铁是负极失去电子而被腐蚀。a和b不连接时,铁与硫酸铜发生置换反应生成铜与硫酸亚铁而被腐蚀,C正确;D、a和b分别连接电源正、负极时,构成电解池。Fe电极是阳极,失去电子,发生的电极反应为:Fe-2e-=Fe2+,D不正确,答案选D。

练习册系列答案
相关题目

 Li1-x MnO2 + LixC6 (LixC6表示锂原子嵌入石墨形成的复合材料)下列有关说法正确的是
Li1-x MnO2 + LixC6 (LixC6表示锂原子嵌入石墨形成的复合材料)下列有关说法正确的是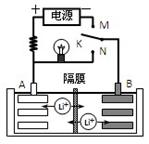
 MgxMo3S4,下列说法错误的是
MgxMo3S4,下列说法错误的是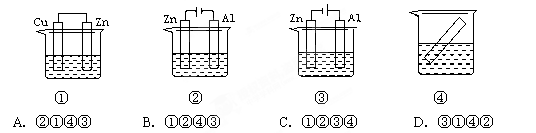
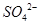 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是