题目内容
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学的知识回答:
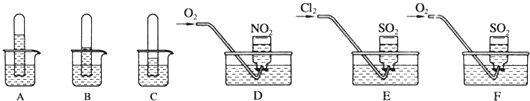
(1)A为0.1 mol/L的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为____________。
(2)B为0.1 mol/L NaHCO3溶液,请分析NaHCO3溶液显碱性的原因:__________________。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时常加入______溶液以抑制其水解,若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为__________________。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:AgCl(s)![]() Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.2 mol/L AgNO3溶液中;③100 mL 0.1 mol/L氯化铝溶液中;④100 mL 0.1 mol/L盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是___________ (填写序号);②中氯离子的浓度为_______mol/L。
Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.2 mol/L AgNO3溶液中;③100 mL 0.1 mol/L氯化铝溶液中;④100 mL 0.1 mol/L盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是___________ (填写序号);②中氯离子的浓度为_______mol/L。
【答案】(1)c(![]() )>c(
)>c(![]() )>c(H+)>c(OH-)(2分)
)>c(H+)>c(OH-)(2分)
(2)![]() 的水解程度大于其电离程度,溶液中c(OH-)>c(H+),故溶液显碱性(2分)
的水解程度大于其电离程度,溶液中c(OH-)>c(H+),故溶液显碱性(2分)
(3)氯化氢(或HCl) (1分) Fe3++3![]()
![]() Fe(OH)3↓+3CO2↑(2分)
Fe(OH)3↓+3CO2↑(2分)
(4)②>①>④>③(2分) 9×10-10(3分)
【解析】(1)(NH4)2SO4溶液中![]() 水解使溶液呈酸性。(2)NaHCO3溶液中
水解使溶液呈酸性。(2)NaHCO3溶液中![]() 的电离程度小于其水解程度,故溶液显碱性。(3)为抑制FeCl3水解常加入盐酸,Fe3+与
的电离程度小于其水解程度,故溶液显碱性。(3)为抑制FeCl3水解常加入盐酸,Fe3+与![]() 可发生相互促进的水解。(4)Ag+浓度与溶液中的Cl-浓度有关,即c(Ag+)·c(Cl-)=Ksp。
可发生相互促进的水解。(4)Ag+浓度与溶液中的Cl-浓度有关,即c(Ag+)·c(Cl-)=Ksp。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案