题目内容
【题目】六种短周期元素,aA、bB、cC、dD、eE、fF,已知原子序数大小关系是:a<e<c<b<f<d,且a+b=(c+d)/2;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻。
(1)B、C、D三种元素形成的六原子核的化合物和水反应的离子方程式是:_______________。
(2)A、C形成的四原子核化合物甲的电子式为_______,该化合物呈弱酸性,试写出这种化合物的电离方程式:_______________。
(3)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:__________________________________________________。
(4)写出A、C、D形成的六原子核化合物乙的水溶液和甲的水溶液反应的化学方程式:_______________________________________________________。
(5)写出E和F形成的化合物和化合物A2C反应的化学方程式:____________。
(6)A、E形成的四原子核化合物丙容易液化,其原因是:___________。
【答案】SO32-+H2O![]() HSO3-+OH-(HSO3-+H2O
HSO3-+OH-(HSO3-+H2O![]() H2SO3+OH-)
H2SO3+OH-) ![]() H2O2
H2O2![]() HO2-+H+ H++HSO3-=SO2↑+H2O H2O2+H2SO3=H2SO4+H2O Mg3N2+6H2O=2NH3↑+3Mg(OH)2↓ 分子间形成氢键,增加了分子之间的作用力,使之易液化
HO2-+H+ H++HSO3-=SO2↑+H2O H2O2+H2SO3=H2SO4+H2O Mg3N2+6H2O=2NH3↑+3Mg(OH)2↓ 分子间形成氢键,增加了分子之间的作用力,使之易液化
【解析】
因为六种元素是短周期元素,由A、B同主族,C、D也同主族,且原子序数a<b,c<d,C、D肯定是第二、第三周期元素,(c+d)/2≤![]() =13,推出A肯定是H元素,由于原子序数b>c,则B元素肯定为Na元素,则有1+11=(c+c+8)/2,解得c=8,即C为O元素,D为S元素,再根据C、E相邻,B、F也相邻及原子序数大小确定E为N元素,F为Mg元素。据此解答。
=13,推出A肯定是H元素,由于原子序数b>c,则B元素肯定为Na元素,则有1+11=(c+c+8)/2,解得c=8,即C为O元素,D为S元素,再根据C、E相邻,B、F也相邻及原子序数大小确定E为N元素,F为Mg元素。据此解答。
(1)B、C、D三种元素形成的六原子核的化合物是亚硫酸钠,在溶液中水解,则和水反应的离子方程式是SO32-+H2O![]() HSO3-+OH-(HSO3-+H2O
HSO3-+OH-(HSO3-+H2O![]() H2SO3+OH-)。
H2SO3+OH-)。
(2)A、C形成的四原子核化合物甲是双氧水,电子式为![]() ,该化合物呈弱酸性,该化合物的电离方程式为H2O2
,该化合物呈弱酸性,该化合物的电离方程式为H2O2![]() HO2-+H+。
HO2-+H+。
(3)分别由A、B、C、D四种元素所形成的两种化合物是亚硫酸氢钠和硫酸氢钠,在水溶液相互反应的离子方程式为H++HSO3-=SO2↑+H2O。
(4)A、C、D形成的六原子核化合物乙是亚硫酸,其水溶液和甲的水溶液反应的化学方程式为H2O2+H2SO3=H2SO4+H2O。
(5)E和F形成的化合物是氮化镁,化合物A2C即水反应的化学方程式为Mg3N2+6H2O=2NH3↑+3Mg(OH)2↓。
(6)A、E形成的四原子核化合物丙是氨气,由于氨气分子间形成氢键,增加了分子之间的作用力,使之易液化。

【题目】下列各组物质中,不能按![]() (“→”表示一步完成)的关系相互转化的是 ( )
(“→”表示一步完成)的关系相互转化的是 ( )
选项 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | Cl2 | NaClO | NaCl |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A.AB.BC.CD.D
【题目】某温度下,H2(g)+CO2(g)![]() H2O(g)+CO2(g)的平衡常数
H2O(g)+CO2(g)的平衡常数![]() 。该温度下在甲、乙、丙三个恒容密闭容器中,
。该温度下在甲、乙、丙三个恒容密闭容器中,
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol | 0.010 | 0.020 | 0.020 |
c(CO2)/mol | 0.010 | 0.010 | 0.020 |
投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是( )
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
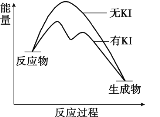
【题目】向20 mL 0.40 mol/L H2O2溶液中加入少量KI溶液:ⅰ.H2O2+I-=H2O+IO﹣;ⅱ.H2O2+IO﹣= H2O+O2↑+ I﹣。H2O2分解反应过程中能量变化和不同时刻测得生成O2的体积(已折算标准状况)如下。
t/min | 0 | 5 | 10 | 15 | 20 |
V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |
下列判断不正确的是
A. 从图中可以看出,KI能增大H2O2的分解速率
B. 反应ⅰ是放热反应,反应ⅱ是吸热反应
C. 0~10 min的平均反应速率:v(H2O2)≈9.0×10-3 mol/(L·min)
D. H2O2在反应过程中既体现了氧化性,又体现了还原性