题目内容
【题目】(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等。
①基态Fe3+的M层电子排布式为__________________。
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_________。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__________(填晶体类型)
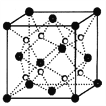
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为__________。已知该晶胞的密度为ρg/cm3,阿伏加德罗常数为NA,求晶胞边长a=__________cm。(用含ρ、NA的计算式表示)
(3)下列说法正确的是__________。
A.第一电离能大小:S>P>Si
B.电负性顺序:C<N<O<F
C.因为晶格能CaO比KCl高,所以KCl比CaO熔点低
D.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
E.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(4)图1是:Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

①图中d单质的晶体堆积方式类型是______________________。
②图2是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:__________________________。
【答案】 3s23p63d5 5 分子晶体 立方体  BC 面心立方最密堆积 硝酸分子是极性分子,易溶于极性溶剂的水中,硝酸分子中氢氧键易与水分子间形成氢键
BC 面心立方最密堆积 硝酸分子是极性分子,易溶于极性溶剂的水中,硝酸分子中氢氧键易与水分子间形成氢键
【解析】(1)①Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5 ,则M层电子排布式为:3s23p63d5,故答案为:3s23p63d5;
②配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5,分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,故答案为:5;分子晶体;
(2)距一个阴离子周围最近的所有阳离子为顶点构成的几何体是立方体,该晶胞中钠离子个数是8,氧离子个数=8/8+6/2=4,V=m/ρ=248/ρNAcm3,则a= ,故答案为:立方体;
,故答案为:立方体;  ;
;
(3)A.同一周期元素中,元素的第一电离能随着原子序数的增大呈增大趋势,但第VA族元素的第一电离能大于相邻元素,所以第一电离能大小:P>S>Si,故A错误;B.同一周期元素中,元素的电负性随着原子序数的增大而增大,所以电负性顺序:C<N<O<F,故B正确;C.晶格能与离子晶体的熔点成正比,离子半径与晶格能成反比,离子所带电荷与晶格能成正比,钙离子电荷大于钾离子,且钙离子半径小于钾离子,氯离子所带电荷小于氧离子,且氯离子半径大于氧离子,所以氯化钾的晶格能小于氧化钙,则氯化钾的熔点比氧化钙低,故C正确;D.二氧化硫分子中硫原子的价层电子对是3且含有一个电子对,所以二氧化硫是V形结构,为极性分子,二氧化碳是非极性分子,根据相似相溶原理知,二氧化硫易溶于水,故D错误;E.分子晶体中,物质的熔沸点与其相对分子质量成正比,故D错误;故选BC;
(4)①d单质是热和电的良导体,且熔点较高,则为铜,铜为面心立方最密堆积,故答案为:面心立方最密堆积;
②根据图知,该分子中含有一个氢原子、三个氧原子和一个氮原子,为硝酸分子,硝酸分子正负电荷重心不重合,为极性分子,且硝酸和水能形成氢键而增大硝酸的溶解性,故答案为:硝酸分子是极性分子,易溶于极性溶剂的水中,硝酸分子中氢氧键易与水分子间形成氢键。