题目内容
将2mol X和2mol Y通入2L密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g)+aQ(g),2min达到平衡时生成0.8mol Z,测得Q的浓度为0.4mol/L,下列叙述错误的是( )
| A、a的值为2 |
| B、化学平衡常数K=0.5 |
| C、平衡时X的浓度为1.6mol/L |
| D、Y的转化率为60% |
考点:化学平衡的计算
专题:化学平衡专题
分析:X(g)+3Y(g) ?2Z(g)+a Q(g)
?2Z(g)+a Q(g)
开始 2 2 0 0
转化 0.4 1.2 0.8 0.4a
平衡 1.6 0.8 0.8 0.4a
v(Z)=
=0.2mol/(L?min),v(Q)=
=0.2mol/(L?min),
结合反应速率之比等于化学计量数之比及化学平衡常数、转化率的计算方法来解答.
 ?2Z(g)+a Q(g)
?2Z(g)+a Q(g)开始 2 2 0 0
转化 0.4 1.2 0.8 0.4a
平衡 1.6 0.8 0.8 0.4a
v(Z)=
| ||
| 2min |
| 0.4mol/L |
| 2min |
结合反应速率之比等于化学计量数之比及化学平衡常数、转化率的计算方法来解答.
解答:
解:X(g)+3Y(g) ?2Z(g)+a Q(g)
?2Z(g)+a Q(g)
开始 2 2 0 0
转化 0.4 1.2 0.8 0.4a
平衡 1.6 0.8 0.8 0.4a
v(Z)=
=0.2mol/(L?min),v(Q)=
=0.2mol/(L?min),
A.
=
,反应速率相同,则a=2,故A正确;
B.化学平衡常数K=
=
=0.5,故B正确;
C.平衡时X的浓度为
=0.8mol/L,故C错误;
D.Y的转化率为
×100%=60%,故D正确;
故选C.
 ?2Z(g)+a Q(g)
?2Z(g)+a Q(g)开始 2 2 0 0
转化 0.4 1.2 0.8 0.4a
平衡 1.6 0.8 0.8 0.4a
v(Z)=
| ||
| 2min |
| 0.4mol/L |
| 2min |
A.
| v(Z) |
| v(Q) |
| 2 |
| a |
B.化学平衡常数K=
| c2(Q)?c2(Z) |
| c(X)c3(Y) |
| 0.42×0.42 |
| 0.43×0.8 |
C.平衡时X的浓度为
| 1.6mol |
| 2L |
D.Y的转化率为
| 1.2mol |
| 2mol |
故选C.
点评:本题考查化学平衡的计算,明确化学平衡三段法计算是解答的关键,注意反应速率与化学计量数的关系及化学平衡常数、转化率的计算方法即可解答,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
如图是两种致癌物质的结构简式,以下的描述正确的是( )
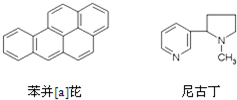

| A、它们都属于烃 |
| B、苯并[a]芘的分子式是C20H12 |
| C、尼古丁的分子式是C10H13N2 |
| D、苯并[a]芘的分子是由5个苯的结构单元并合而成,所以它是苯的同系物 |
下列说法正确的是( )
| A、脂肪烃、芳香烃和卤代烃都属于烃 |
| B、天然气、沼气和水煤气都属于可再生的清洁能 |
| C、工业上分别用热还原法、热分解法和电解法冶炼铜、镁和铝 |
| D、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
下列电离方程式中正确的是( )
| A、Na2HPO4溶于水:Na2HPO4=2Na++H++PO43- |
| B、NaHSO4熔化:NaHSO4=Na++H++SO42- |
| C、HF溶于少量水中:2HF=H++HF2- |
| D、(NH4)2 SO4溶于水:(NH4)2 SO4=2 NH4++SO42一 |
 标准状况下,某同学向100mL H2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )
标准状况下,某同学向100mL H2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )| A、亚硫酸的酸性比氢硫酸的酸性弱 |
| B、ab段反应是:SO2+2H2S═3S↓+2H2O |
| C、原H2S溶液的物质的量浓度为0.05mol/L |
| D、b点对应的溶液导电性最强 |
下列有机物中,含有两种官能团的是( )
| A、CH3-CH2-Cl |
B、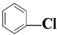 |
| C、CH2=CHBr |
D、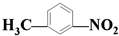 |
(双选)下列物质中互为同分异构体的是( )
A、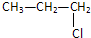 |
B、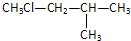 |
C、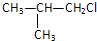 |
| D、CH3CH2CH2CH2Cl |
下列各组物质中,仅用水及物质间相互反应不能一一区别的一组是( )
| A、Na2O2 Al2(SO4)3 MgCl2 K2CO3 |
| B、BaCl2 Na2SO4 (NH4)SO4 KOH |
| C、AgNO3 NaCl KCl CuCl2 |
| D、Fe2(SO4)3 K2CO3 KHSO4 NH4Cl |
下列实验操作中一定会造成误差的是( )
| A、将pH试纸用蒸馏水湿润后测某溶液的pH |
| B、在中和热的测定实验中用Ba(OH)2代替NaOH;H2SO4代替HCl |
| C、用碱石灰来干燥氨气 |
| D、使用托盘天平称量时将药品放在天平的右盘与砝码放在天平的左盘 |