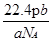题目内容
用表示阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol Na2O2晶体中共含有个离子 |
| B.0.1 molAlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| C.常温常压下,和混合气体含有个氧原子 |
| D.电解法冶炼铝时每转移个电子,阳极生成氧气 |
C
解析

练习册系列答案
相关题目
下列有关化学用语的表示方法中正确的是( )
A.氯元素的原子结构示意图: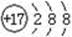 | B.N2的结构式:N≡N |
C.原子核内有8个中子的氧原子: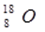 | D.二氧化碳的电子式: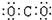 |
下列说法不正确的是
| A.互为同分异构体的分子结构几乎完全相同 |
| B.丙氨酸CH3-CH(NH2)-COOH存在手性异构体 |
| C.标准状况下,相同体积的NH3 、CH4、HF含有相同的电子数 |
| D.等体积的CO和N2混合后所得的混合气体的平均摩尔质量为28 g/mol |
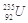 是重要的核工业原料,在自然界的含量很低,它的浓缩一直为国际社会所关注。下面列出该原子核内中子数与核外电子数之差的数据正确的是
是重要的核工业原料,在自然界的含量很低,它的浓缩一直为国际社会所关注。下面列出该原子核内中子数与核外电子数之差的数据正确的是
| A.51 | B.92 | C.143 | D.235 |
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5
则下列有关比较中正确的是
| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高正化合价:④>③=②>① |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.4.0 g重水(D2O)中所含中子数为1.6 NA |
| B.1 L 2 mol·L-1 K2S溶液中S2-和HS-的总数为2 NA |
| C.2.4g金刚石与石墨的混合物中所含碳原子数为0.2 NA |
| D.50 mL 18 mol·L-1浓硫酸与足量铜反应,转移的电子数为0.9 NA |
NA代表阿伏加德罗常数,下列说法错误的是
| A.标准状况下,22.4 L NO和22.4 L O2的混合,混合气体中含有的氧原子数为3NA |
| B.0.012 kg 13C中,含中子数为7NA |
| C.25 ℃时,1 L pH=13的氢氧化钡溶液中含有0.1NA个氢氧根离子 |
D.在反应3SiO2+6C+2N2  Si3N4+6CO,生成1 mol Si3N4时共转移12 NA电子 Si3N4+6CO,生成1 mol Si3N4时共转移12 NA电子 |
我国稀土矿资源丰富,品位甚高。提取稀土元素可以向含RE(RE表示稀土元素)的硫酸盐溶液中加入粉状Na2SO4,使稀土元素转入沉淀。有关的反应为(RE)2(SO4)3+Na2SO4+xH2O (RE)2(SO4)3·Na2SO4·xH2O↓。下列叙述不正确的是( )
(RE)2(SO4)3·Na2SO4·xH2O↓。下列叙述不正确的是( )
| A.该反应属于化合反应 |
| B.该反应属于可逆反应 |
| C.生成的产物在分类上属于复盐 |
| D.RE在化合物中的化合价为+3 |
 B
B 
 D
D