题目内容
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2
| A.只有②③④⑤ | B.只有①②⑤ | C.只有②③⑤ | D.全部 |
A
解析试题分析:①金属钠投入到FeCl3溶液中,得到红褐色沉淀;②过量Ba(OH)2溶液和明矾溶液混合,生成BaSO4白色沉淀;③少量Ca(OH)2投入过量NaHCO3溶液中,生成CaCO3白色沉淀;④向NaAlO2溶液中通入过量CO2,生成Al(OH)3白色沉淀;⑤向饱和Na2CO3溶液中通入足量CO2,生成溶解度更小的NaHCO3,会析出白色的NaHCO3,故A项正确。
考点:本题考查物质的化学性质和反应现象的判断。

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
下列实验中,溶液颜色有明显变化的是( )
| A.少量明矾溶液加入到过量NaOH溶液中 |
| B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C.少量Na2O2固体加入到过量NaHSO3溶液中 |
| D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液 |
下列说法正确的是
| A.铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
| B.硅在电子工业中是最重要的半导体材料,广泛用于制作光导纤维 |
| C.二氧化硫是一种有毒气体,所以不能用于杀菌消毒 |
| D.氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 |
下列实验的现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有吸水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)
| A.图1:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
用4种溶液进行实验,下表中“操作及现象”与“溶液”不符的是
| 选项 | 操作及现象 | 溶液 |
| A | 通入SO2,溶液不变浑浊,再加氯水,变浑浊 | BaCl2溶液 |
| B | 通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| C | 通入SO2,溶液变浑浊,继续通SO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 | Ca(OH)2溶液 |
| D | 通入NH4HCO3受热分解产生的气体,溶液变浑浊,继续通入该气体,浑浊消失 | Ca(OH)2溶液 |
下列物质转化在给定条件下能实现的是
①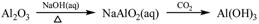
②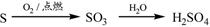
③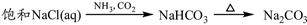
④
⑤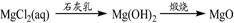
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物: |
B.Fe在Cl2中的燃烧产物: |
C.AlCl3溶液中滴加NaOH后铝的存在形式: |
D.氨水与SO2反应后溶液中的铵盐: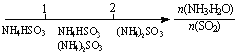 |
氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质丙和6.72 LH2(已折算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物M,该物质溶于氢氧化钠溶液。化合物乙是工业制取硝酸的原料之一,乙在催化剂存在下可分解得到H2和另一种单质气体丁。下列说法正确的是( )
| A.工业上制备单质丙的方法是电解其氯化物 |
| B.丙丁元素形成化合物可用于制作新型陶瓷 |
| C.甲与水的反应中,水做还原剂 |
| D.单质丙也可以与氢氧化钠反应,并生成白色沉淀物M |