题目内容
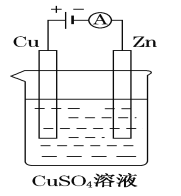
【题目】烧杯A中盛放0.1 mol·L-1的H2SO4溶液,烧杯B中盛放0.1 mol·L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )

A.A为原电池,B为电解池
B.A中阳离子向碳极移动,阴离子向铁极移动
C.当A烧杯中产生0.1 mol气体时,B烧杯中产生气体的物质的量也为0.1 mol
D.一段时间后,B烧杯中溶液的浓度增大
【答案】D
【解析】
试题分析:A、根据装置图,A装置为原电池,B为电解池,故说法正确;B、Fe作负极,A中石墨作正极,根据原电池的工作原理,阳离子向正极移动,阴离子向负极移动,故说法正确;C、A中正极:2H++2e-=H2↑,B装置中左端C连接原电池的负极,作阴极,电极反应式:Cu2++2e-=Cu,右端C连接原电池中正极,作阳极,电解反应式:2Cl-2e-=Cl2↑,n(H2)=n(Cl2),故说法正确;D、B装置中电解CuCl2,溶质的物质的量降低,浓度减小,故说法错误。

练习册系列答案
相关题目