题目内容
在一定条件下,氯气可以与氯化铵发生如下反应:xCl2+yNH4Cl==yNClx+(x+y)HCl,当消耗6.72L(标准状况)的氯气时,生成0.1mol氮的氯化物,则此氮的氯化物的化学式为
| A.NCl2 | B.NCl3、 | C.NCl4 | D.NCl5 |
B
当消耗6.72L(标准状况)的氯气,即0.3molCl2时,生成0.1mol氮的氯化物,由原子守恒得:Cl: 2x+y=xy+x+y,H :4y=x+y,解得:x=3,y=1,选B。

练习册系列答案
相关题目
 调控。
调控。 装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。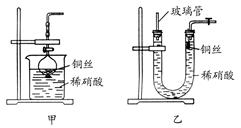
 状况下________mL O2才能使NO全部溶于水。
状况下________mL O2才能使NO全部溶于水。 (1)维生素C又称抗坏血酸,其水溶液显酸性。向维生素C的溶液中滴加紫色石蕊溶液,溶液变 色。
(1)维生素C又称抗坏血酸,其水溶液显酸性。向维生素C的溶液中滴加紫色石蕊溶液,溶液变 色。 ② KI溶液 ③酸性KMnO4溶液
② KI溶液 ③酸性KMnO4溶液 ② KI ③ KIO3
② KI ③ KIO3 O3
O3 求回答下列问题:
求回答下列问题: