题目内容
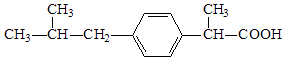
【题目】今有化合物: 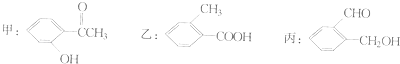
(1)请写出丙中含氧官能团的名称:;
(2)请判别上述哪些化合物互为同分异构体:;
(3)请分别写出鉴别甲、乙、丙化合物的方法.(指明所选试剂及主要现象即可) 鉴别甲的试剂:;现象:;
鉴别乙的试剂:;现象:;
鉴别丙的试剂:;现象: .
【答案】
(1)醛基、羟基
(2)甲、乙、丙
(3)氯化铁溶液;溶液为紫色;新制氢氧化铜;蓝色溶液;新制氢氧化铜;砖红色沉淀
【解析】解:(1)丙含有的官能团为醛基和羟基,所以答案是:醛基、羟基;(2)甲、乙、丙分子式都为C8H8O2 , 但结构不同,主要是官能团不同,互为同分异构体,所以答案是:甲、乙、丙;(3)鉴别甲可利用氯化铁溶液,显紫色,而乙、丙中分别加新制氢氧化铜,得到蓝色溶液的为乙,生成砖红色沉淀的为丙, 所以答案是:氯化铁溶液,溶液为紫色;新制氢氧化铜,蓝色溶液;新制氢氧化铜,砖红色沉淀.
【考点精析】根据题目的已知条件,利用有机物的结构和性质的相关知识可以得到问题的答案,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解.

【题目】自然界中,金属元素大多以化合态存在,通过金属冶炼得到金属单质.工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但生产钾是用金属钠和熔化的KCl在一定的条件下反应制取:KCl+NaNaCl+K+Q (Q<0) 有关数据如表:
熔点℃ | 沸点℃ | 密度 (g/cm3) | |
Na | 97.8 | 882.9 | 0.97 |
K | 63.7 | 774 | 0.86 |
NaCl | 801 | 1413 | 2.165 |
KCl | 770 | 1500 | 1.984 |
(1)请结合平衡移动理论分析,为什么能用该反应制备金属钾. .
(2)在常压下金属钾转为气态从反应混合物中分离的最低温度约为℃,而反应的最高温度应低于℃.
(3)在制取金属钾的过程中,为了提高原料的转化率可采取的措施有 . (任写两点)
(4)相比于电解熔融氯化钾,此方法的优点有
(5)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为k=