题目内容
某工厂排放的废水中含有游离的氯,为了除去游离氯,且使废水变为中性,有人提出如下图方案,在废水排出口的A、B处分别注入一定流量的废烧碱溶液和亚硫酸钠溶液,已知Cl2与Na2SO3发生反应:Cl2+Na2SO3+H2O====2HCl+Na2SO4。

试写出:
(1)A、B处应加入的物质分别是:A___________,B___________。(写化学式)
(2)写出反应的离子方程式:A___________________________,
B____________________________________________________________。

试写出:
(1)A、B处应加入的物质分别是:A___________,B___________。(写化学式)
(2)写出反应的离子方程式:A___________________________,
B____________________________________________________________。
(1)Na2SO3 NaOH
(2)Cl2+ +H2O====2H++2Cl-+
+H2O====2H++2Cl-+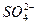 H++OH-====H2O
H++OH-====H2O
(2)Cl2+
 +H2O====2H++2Cl-+
+H2O====2H++2Cl-+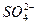 H++OH-====H2O
H++OH-====H2O题目要求除去游离氯(Cl2),且使废水变为中性,Cl2具有强氧化性,用还原剂Na2SO3除去,根据题给信息,Cl2与Na2SO3反应后产生酸液,可用废烧碱(NaOH)中和,因此上游A处应加入Na2SO3,下游B处加入废烧碱。

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目


 H++
H++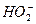 )消耗了OH-,而使酚酞褪色;乙同学认为,过氧化氢具有强氧化性,将酚酞氧化,红色消失。试设计一个简单易行的实验验证甲、乙两同学的解释哪个正确。
)消耗了OH-,而使酚酞褪色;乙同学认为,过氧化氢具有强氧化性,将酚酞氧化,红色消失。试设计一个简单易行的实验验证甲、乙两同学的解释哪个正确。