题目内容
根据化学学科中的基本理论,请回答下列问题:
Ⅰ、常温下,取pH=2的盐酸和醋酸溶液各100 ml, 向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是_____ (填“A”或“B”)。

Ⅱ、丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l),△H1=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2=-566kJ/mol
(1)写出丙烷的燃烧热的热化学方程式: 。
(2)现有1mol C3H8在不足量的氧气里燃烧,生成1mol CO和2mol CO2以及气态水,将所有的产物通入一个固定体积为1L的密闭容器中,在一定条件下发生如下可逆反应:
CO(g)+H2O(g)=CO2(g)+ H2(g) △H1=+41.2kJ/mol
①下列事实能说明该反应达到平衡的是
a.体系中的压强不发生变化 b.v正(H2)=v逆(CO)
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再反生变化
②5min后体系达到平衡,经测定,H2为0.8mol,则v(H2)= 。
③向平衡体系中充入少量CO,则平衡常数 (填“增大”、“减小”或“不变”)。
(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-。在电池内部O2-移向 极(填“正”或“负”);电池的正极电极反应为 。
Ⅰ、常温下,取pH=2的盐酸和醋酸溶液各100 ml, 向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是_____ (填“A”或“B”)。

Ⅱ、丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l),△H1=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2=-566kJ/mol
(1)写出丙烷的燃烧热的热化学方程式: 。
(2)现有1mol C3H8在不足量的氧气里燃烧,生成1mol CO和2mol CO2以及气态水,将所有的产物通入一个固定体积为1L的密闭容器中,在一定条件下发生如下可逆反应:
CO(g)+H2O(g)=CO2(g)+ H2(g) △H1=+41.2kJ/mol
①下列事实能说明该反应达到平衡的是
a.体系中的压强不发生变化 b.v正(H2)=v逆(CO)
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再反生变化
②5min后体系达到平衡,经测定,H2为0.8mol,则v(H2)= 。
③向平衡体系中充入少量CO,则平衡常数 (填“增大”、“减小”或“不变”)。
(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-。在电池内部O2-移向 极(填“正”或“负”);电池的正极电极反应为 。
Ⅰ、B (2分)
Ⅱ、(1)C3H8(g)+5O2(g)==3CO2(g)+4H2O(l),△H=-2219.9KJ/mol (2分)
(2)①b、d;(2分)②0.16 mol/L?min;(2分) ③不变 (2分)
(3)负极(1分), O2+4e- = 2O2-(2分)
Ⅱ、(1)C3H8(g)+5O2(g)==3CO2(g)+4H2O(l),△H=-2219.9KJ/mol (2分)
(2)①b、d;(2分)②0.16 mol/L?min;(2分) ③不变 (2分)
(3)负极(1分), O2+4e- = 2O2-(2分)
试题分析:Ⅰ、醋酸是弱酸,存在电离平衡,盐酸是强酸,全部电离,因此在pH相等的条件下醋酸溶液的浓度大于盐酸溶液的浓度。与锌的反应过程中醋酸还可以继续电离出氢离子,所以醋酸与锌反应的速率大,因此表示醋酸溶液中pH变化曲线的是B。
Ⅱ、(1)已知①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l),△H1=-2741.8kJ/mol、②2CO(g)+O2(g)=2CO2(g) △H2=-566kJ/mol,则依据盖斯定律可知(①+②×3)÷2即得到热化学方程式C3H8(g)+5O2(g)==3CO2(g)+4H2O(l),其中△H=(-2741.8kJ/mol-566kJ/mol×3)÷2=-2219.9KJ/mol。
(2)①a.由反应可知,反应前后的压强始终不变,则体系中的压强不发生变化,不能判断平衡,故a错误;b.v正(H2)=v逆(CO),说明正逆反应速率相等,故b正确;c.因体积不变,气体的总质量不变,所以混合气体的平均相对分子质量始终不变,不发生变化,不能判断平衡,故c错误;d.CO2的浓度不再发生变化,由平衡的特征“定”可知,则化学反应达到平衡,故d正确;故答案为:bd;
②5min后达到平衡,H2为0.8mol,其浓度是0.8mol÷1L=0.8mol/L,则v(H2)=0.8mol/L÷5min=0.16mol/(L?min);
③因平衡常数与温度有关,温度不变,平衡常数不变;
(3)原电池内部阴离子向由正极向负极移动,所以电池内部O2-由正极移向负极;原电池负极失去电子发生氧化反应,丙烷在负极放电,与O2-结合生成二氧化碳与水,电极反应式为C3H8+10O2--20e-=3CO2+4H2O,正极是氧气得到电子,发生还原反应,电极反应式为O2+4e- =2O2-。

练习册系列答案
相关题目
 4NO(g)+6 H2O(g)△H。
4NO(g)+6 H2O(g)△H。
 4NO(g)+6 H2 O(g)达到平衡状态的是 (填序号)。
4NO(g)+6 H2 O(g)达到平衡状态的是 (填序号)。


 2SO3(g)ΔH="-197" kJ·mol-1。实验测得4 mol SO2参加上述反应放出354 kJ热量,则SO2的转化率最接近于( )
2SO3(g)ΔH="-197" kJ·mol-1。实验测得4 mol SO2参加上述反应放出354 kJ热量,则SO2的转化率最接近于( ) CO2(g) + 3H2(g) ;△H>0
CO2(g) + 3H2(g) ;△H>0

 =____________(写出表达式即可)。
=____________(写出表达式即可)。 2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断: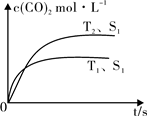
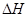 =-867kJ·mol-1
=-867kJ·mol-1 N2O4(g)
N2O4(g) 