题目内容
【题目】钴酸锂废极片中钴回收的某种工艺流程如下图所示,其中废极片的主要成分为钴酸锂(LiCoO2)和金属铝,最终可得到Co2O3及锂盐。

(1) “还原酸浸”过程中,大部分LiCoO2可转化为CoSO4,请将该反应的化学方程式补充完整:2LiCoO2+3H2SO4+□ ![]() □CoSO4+□ +□ + □ 。__________
□CoSO4+□ +□ + □ 。__________
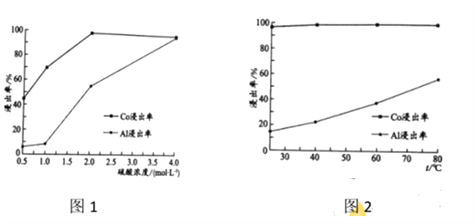
(2) “还原酸浸”过程中,Co、Al浸出率(进入溶液中的某元素质量占固体中该元素总质量的百分数)受硫酸浓度及温度(t)的影响分别如图1和图2所示。工艺流程中所选择的硫酸浓度为2 mol.L-1,温度为80 oC,推测其原因是________。
A. Co的浸出率较高 B. Co和Al浸出的速率较快
C. Al的浸出率较高 D. 双氧水较易分解
(3)加入(NH4)2C2O4后得CoC2O4沉淀。写出CoC2O4沉淀在空气中高温煅烧得到Co2O3的反应的化学方程式:________。
(4)若初始投入钴酸锂废极片的质量为1 kg,煅烧后获得Co2O3的质量为83 g,已知Co的浸出率为90%,则钴酸锂废极片中钴元素的质量分数约为________(小数点后保留两位)。
(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10-1 mol·L-1,部分锂盐的溶解度数据如下表所示。
温度 | Li2SO4 | Li2CO3 |
0 oC | 36.1 g | 1.33 g |
100 oC | 24.0 g | 0.72 g |
结合数据分析,沉锂过程所用的试剂b是________(写化学式),相应的操作方法:向滤液a中加入略过量的试剂b,搅拌,________,洗涤干燥。
【答案】 2LiCoO2 + 3H2SO4 + H2O2![]() 2CoSO4 + Li2SO4 + O2↑+ 4H2O A B 4CoC2O4 + 3O2
2CoSO4 + Li2SO4 + O2↑+ 4H2O A B 4CoC2O4 + 3O2![]() 2Co2O3 + 8CO2 6.56 % Na2CO3 加热浓缩,趁热过滤
2Co2O3 + 8CO2 6.56 % Na2CO3 加热浓缩,趁热过滤
【解析】(1). “还原酸浸”过程中,大部分LiCoO2可转化为CoSO4,Co元素的化合价从+3价降低到+2价,则H2O2中O元素的化合价从-1价升高到0价,根据得失电子守恒和原子守恒,该反应的化学方程式为:2LiCoO2 + 3H2SO4 + H2O2= 2CoSO4 + Li2SO4 + O2↑+ 4H2O,故答案为:2LiCoO2 + 3H2SO4 + H2O2= 2CoSO4 + Li2SO4 + O2↑+ 4H2O;
(2). 由图1可知,当硫酸浓度为2 mol.L-1时,Co的浸出率较高,由图2可知,当温度为80℃,Co和Al浸出的速率较快,故答案选:AB;
(3). CoC2O4沉淀在空气中高温煅烧,CoC2O4被氧气氧化得到Co2O3,反应的化学方程式为:4CoC2O4 + 3O2= 2Co2O3 + 8CO2,故答案为:4CoC2O4 + 3O2= 2Co2O3 + 8CO2;
(4). 煅烧后获得Co2O3的质量为83 g,则Co原子的质量为:83×![]() =59g,Co的浸出率为90%,则1 kg钴酸锂废极片中钴元素的质量分数约为
=59g,Co的浸出率为90%,则1 kg钴酸锂废极片中钴元素的质量分数约为![]() ×100%=6.56 %,故答案为:6.56 %;
×100%=6.56 %,故答案为:6.56 %;
(5). 由表中数据可知,在相同温度下,Li2CO3的溶解度更小,且温度越高,Li2CO3的溶解度越小,则沉锂过程所用的试剂b是Na2CO3,相应的操作方法:向滤液a中加入略过量的Na2CO3,搅拌,加热浓缩,趁热过滤,洗涤干燥,故答案为:Na2CO3;加热浓缩,趁热过滤。