题目内容
下列化学用语的理解正确的是( )
| A、29Cu的价电子排布式为3d94s2 |
| B、HClO的结构式:H-Cl-O |
C、比例模型  ,可以同时表示CH4和CCl4分子 ,可以同时表示CH4和CCl4分子 |
| D、1s22s22p3 和 1s22s22p4能形成AB2型共价化合物 |
考点:原子核外电子排布,结构式,球棍模型与比例模型
专题:化学用语专题
分析:A.违背洪特规则特例;
B.根据稳定结构,O原子与H原子、Cl原子之间分别形成1对共用电子对;
C.C原子半径比Cl原子半径小;
D.1s22s22p3 和 1s22s22p4分别表示N、O元素.
B.根据稳定结构,O原子与H原子、Cl原子之间分别形成1对共用电子对;
C.C原子半径比Cl原子半径小;
D.1s22s22p3 和 1s22s22p4分别表示N、O元素.
解答:
解:A.根据洪特规则特例,29Cu的价电子排布式为3d104s1为,故A错误;
B.根据稳定结构,O原子与H原子、Cl原子之间分别形成1对共用电子对,HClO的结构式为H-O-Cl,故B错误;
C.C原子半径比Cl原子半径小,比例模型 不能表示CCl4分子,故C错误;
不能表示CCl4分子,故C错误;
D.1s22s22p3 和 1s22s22p4分别表示N、O元素,二者可以形成共价化合物NO2,故D正确,
故选D.
B.根据稳定结构,O原子与H原子、Cl原子之间分别形成1对共用电子对,HClO的结构式为H-O-Cl,故B错误;
C.C原子半径比Cl原子半径小,比例模型
 不能表示CCl4分子,故C错误;
不能表示CCl4分子,故C错误;D.1s22s22p3 和 1s22s22p4分别表示N、O元素,二者可以形成共价化合物NO2,故D正确,
故选D.
点评:本题考查核外电子排布、结构式、比例模型等常用化学用语,B、C选项为易错点,B中学生容易受HClO分子式影响,C中学生容易考虑空间结构,而忽略原子大小,难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
元素A原子的2P轨道上有2个未成对电子,元素B的3P轨道上也有2个未成对电子,A、B两元素的单质互相反应可生成BA2型化合物,该化合物在通常情况下为气态,则此化合物的相对分子质量为( )
| A、44 | B、60 | C、64 | D、76 |
某有机物的结构简式如图所示,下列说法不正确的是( )
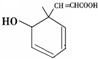

| A、分子式为C10H12O3 |
| B、含有3种官能团 |
| C、1mol该分子中含有3mol双键 |
| D、既可以发生取代反应又可以发生加成反应 |
化学与生产、生活密切相关.下列叙述正确的是( )
| A、碘的升华、溴水中萃取溴、石油的分馏、煤的干馏均是物理变化 |
| B、BaSO4难溶于水是弱电解质,在医学上用作钡餐 |
| C、14C可用于文物年代的鉴定,14C与12C互为同位素 |
| D、明矾和氯气均用于水的消毒、杀菌 |
下列试剂中,能用于检验酒精中是否含有水的是( )
| A、CuSO4?5H2O |
| B、CuSO4 |
| C、金属钠 |
| D、浓硫酸 |
下列有关阴离子的说法正确的是( )
①阴离子一定是酸根离子
②只有活泼的非金属元素才能形成阴离子
③阴离子中不能含有金属元素
④C、Si等第ⅣA族元素的原子很难得电子也就难形成简单阴离子.
①阴离子一定是酸根离子
②只有活泼的非金属元素才能形成阴离子
③阴离子中不能含有金属元素
④C、Si等第ⅣA族元素的原子很难得电子也就难形成简单阴离子.
| A、①②③④ | B、①④ |
| C、①②④ | D、④ |
0.1mol/L KHSO4和0.1mol/L Na2S溶液等体积混合后,溶液能使pH试纸变蓝,则离子浓度关系不正确的是( )
| A、c(SO42-)>c(HS-)>c(OH-)>c(H+) |
| B、c(Na+)=c(S2-)+c(H2S)+c(HS-)+c(SO42-) |
| C、c(Na+)+c(K+)+c(H+)=2c(SO42-)+2c(S2-)+c(HS-)+c(OH-) |
| D、c(Na+)>c(K+)>c(H+)>c(OH-) |
下列有关碱金属元素的叙述正确的是( )
| A、碱金属单质均为银白色,密度均小于水 |
| B、碱金属单质从Li到Cs,熔点依次升高 |
| C、氢氧化铯碱性强于氢氧化钠 |
| D、碱金属元素形成的阳离子,从Li+到Cs+氧化性依次增强 |