题目内容
【题目】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用氯气.
I.工业上通常采用电解法制氯气:观察下图,回答:
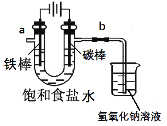
(1)电解反应的化学方程式为____________________。
(2)饱和食盐水通电后,b端产生的气体检验方法是____________。
II. 实验室用NaOH固体配制100 mL 1.0 mol·L-1的NaOH溶液,试回答下列各题:
(3)需要用托盘天平称量_______g NaOH固体;
(4)实验室有下列仪器:①漏斗 ②200mL容量瓶 ③烧杯 ④玻璃棒 ⑤药匙 ⑥托盘天平 ⑦冷凝。若要实施溶液配制,尚缺的玻璃仪器是___________、________;
(5)容量瓶在使用前必须先____________;
(6)配制过程有以下操作: ①称量 ②移液 ③冷却 ④洗涤 ⑤定容 ⑥溶解 ⑦摇匀 其正确的操作顺序应是:① →_________→________ →________ →________→________→ ⑦
(7)下列五项操作中会导致所得溶液浓度偏低的有____________(填序号);
①没有洗涤烧杯内壁和玻璃棒
②未冷却到室温就将溶液转移到容量瓶并定容
③在转移过程中有溶液撒在外面
④定容时观察液面时俯视
⑤定容后,把容量瓶反复摇匀后发现液面低于刻度线,便滴加几滴水至刻度处
【答案】2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 移走烧杯,将湿润的淀粉碘化钾试纸放在b导气管口出,若试纸变蓝,则说明产生的气体为Cl2 4.0 100mL容量瓶 胶头滴管 检查容量瓶是否完好以及瓶塞处是否漏水或检漏 ⑥ ③ ② ④ ⑤ ①③⑤
2NaOH+H2↑+Cl2↑ 移走烧杯,将湿润的淀粉碘化钾试纸放在b导气管口出,若试纸变蓝,则说明产生的气体为Cl2 4.0 100mL容量瓶 胶头滴管 检查容量瓶是否完好以及瓶塞处是否漏水或检漏 ⑥ ③ ② ④ ⑤ ①③⑤
【解析】
(1)在工业上用电解饱和食盐水的方法制取氯气;
(2)电解时与电源正极连接的电极为阳极,阳极发生氧化反应,与电源负极连接的电极为阴极,阴极发生还原反应。根据Cl2与KI发生置换反应,I2遇淀粉溶液变为蓝色检验Cl2。
(3)根据n=c·V及m=n·M计算NaOH的质量;
(4)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
(5)根据容量瓶的作用及溶液特点分析;
(6)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,据此排序;
(7)分析操作对溶质的物质的量和溶液体积的影响,依据c=![]() 进行误差分析。
进行误差分析。
I.(1)电解饱和食盐水的方法制取氯气,反应的化学方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(2)根据图示可知,b端连接电源的正极,为阳极,在阳极,溶液中的阴离子放电。由于阴离子的放电能力Cl->OH-,所以b端发生反应2Cl--2e-=Cl2↑;b端产生的气体是Cl2,该物质具有强的氧化性,与KI在溶液中发生反应:Cl2+2KI=2KCl+I2,I2遇淀粉溶液变为蓝色,所以检验Cl2方法是移走烧杯,将湿润的淀粉碘化钾试纸放在b导气管口处,若试纸变蓝,则说明产生的气体为Cl2。
(3)要配制100 mL 1.0 mol/L的NaOH溶液,根据n=c·V可知:n(NaOH)=1.0mol/L×0.1L=0.1mol,则需要称量NaOH的质量m=n·M=0.1mol×40g/mol=4.0g;
(4)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,需要使用的仪器有托盘天平、药匙、烧杯、量筒、玻璃棒、一定规格的容量瓶、胶头滴管,配制100mL1.0mol/L的NaOH溶液,应选择100mL容量瓶,所以还缺少的仪器:100mL容量瓶、胶头滴管;
(5)容量瓶是准确配制一定体积一定物质的量浓度溶液的仪器,由于溶液检验均一性,溶液各处的浓度相同,在配制溶液时要摇匀溶液,所以在使用前必须先检查容量瓶是否完好以及瓶塞处是否漏水或检漏;
(6)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,所以其正确的操作顺序应是①⑥③②④⑤⑦;
(7)①没有洗涤烧杯内壁和玻璃棒,使溶质的质量减少,n减小,则c偏低,①符合题意;
②未冷却到室温就将溶液转移到容量瓶并定容,等溶液恢复至室温后,液面低于刻度线,V偏小,则溶液浓度偏高,②不符合题意;
③在转移过程中有溶液撒在外面,使n偏少,则导致配制的溶液浓度偏低,③符合题意;
④定容时观察液面时俯视,则V偏小,使物质的量浓度偏高,④不符合题意;
⑤定容后,把容量瓶反复摇匀后发现液面低于刻度线,便滴加几滴水至刻度处,对溶液进行了稀释,使溶液浓度偏低,⑤符合题意;
故正确选项是①③⑤。

【题目】(一)镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。已知:SeO2在常温下是白色的晶体,熔点为340-350℃,则SeO2晶体属于____晶体,SeO2中Se原子采取的杂化类型为___。
(二)A、X、Y、Z、W、M、G等原子序数一次增大的前四周期元素
元素 | 相关信息 |
A | 原子核外电子总数与其周期数相同 |
X | 其羞态原子的L层中有3个未成对电子 |
Y | 荃态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反 |
Z | 原子核外p电子数比s电子数多l个 |
W | 原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817 I3=2745 I4=11575 |
M | 元素的主族数与周期数相差4 |
G | 其基态原子最外层电子数为1,其余各电子层均充满电子 |
(1)画出W基态原子的核外电子排布图______。
(2)A2Y的VSEPR模型名称为____。
(3)已知为X2Y分子中Y原子只与一个X原子相连,请根据等电子原理,写出X2Y的电子式____。
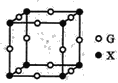
(4)X、G形成的某种化合物的晶胞结构如图所示,则其化学式为______。
(5)已知Z和M形成的化合物的晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的Z离子中心间距离为_____cm。