题目内容
【题目】某科研小组取用0.2 L营养液进行实验。该营养液中含有KCl、K2SO4、NH4Cl三种溶质,测得该营养液中部分离子的浓度如下表所示。
离子符号 | K+ | SO | Cl- |
物质的量浓度(mol·L-1) | 9.0 | 4.0 | 9.0 |
(1)该营养液中K2SO4的物质的量浓度为________,含溶质KCl的质量为________。
(2)该营养液中NH4Cl的物质的量为________。
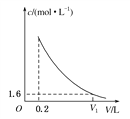
(3)该营养液加水稀释的过程中测得溶液中NH![]() 的物质的量浓度(c)随溶液体积(V)变化的曲线如图所示,则V1为________L。此时营养液中KCl的物质的量浓度为________。
的物质的量浓度(c)随溶液体积(V)变化的曲线如图所示,则V1为________L。此时营养液中KCl的物质的量浓度为________。
【答案】 4 mol·L-1 14.9 g 1.6 mol 1 0.2 mol·L-1
【解析】(1)硫酸根离子物质的量浓度为4.0mol/L,则硫酸钾的物质的量浓度为:c(K2SO4)=c(SO42-)=4.0mol/L;根据钾离子守恒可知,c(K+)=c(KCl)+2c(K2SO4),则c(KCl)=c(K+)-2c(K2SO4)=9.0mol/L-4.0mol/L×2=1.0mol/L,溶质氯化钾的质量为:m(KCl)=McV=74.5g/mol×1.0mol/L×0.2L=14.9g;(2)根据氯原子守恒可知,c(Cl-)=c(KCl)+c(NH4Cl),则:c(NH4Cl)=c(Cl-)-c(KCl)=9.0mol/L-1.0mol/L=8.0mol/L,
氯化铵的物质的量为:n(NH4Cl)=8.0mol/L×0.2L=1.6mol;(3)据c=n/V可知V=n/c,V1=n/c1=1.6mol÷1.6mol/L=1L,此时营养液中KCl的物质的量浓度为0.2mol÷1L=0.2mol/L。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目